Болезнь гоше что это такое видео
СодержаниеЛизосомные болезни накопленияОбразование клеток ГошеГены и болезнь ГошеЭтносы и генетика: миф о «еврейской» болезниКак проявляется болезнь Гоше?Три формы болезни ГошеМожно ли вылечить болезнь Гоше?
Среди орфанных заболеваний болезнь Гоше занимает особое место. Это самая распространенная из лизосомных болезней накопления — патологий, связанных с невозможностью организма избавиться от некоторых веществ. MedAboutMe рассказывает, что это за болезнь и каковы риски получить такой диагноз для обычного человека.
Лизосомные болезни накопления
В каждой клетке постоянно происходят процессы созидания и распада, строительства и утилизации. И существуют специальные органеллы — лизосомы, занимающиеся расщеплением различных деталей клетки, которые по той или иной причине организму больше не нужны. В лизосомах содержится бульон из различных ферментов, каждый из который предназначен для переработки определенного вида веществ. Если каких-то конкретных ферментов нет, их слишком мало или они дефектные, вещества, которые должны были ими перерабатываться, начинают накапливаться внутри клетки. Именно поэтому целая группа заболеваний (около 40) получила название лизосомных болезней накопления (ЛБН). В среднем, у пациентов, страдающих ЛБН, активность определенных лизосомальных ферментов не превышает 10-20% от нормального уровня.
Отложение вещества внутри клетки приводит к постепенному ее разрушению, а значит — к повреждению и разрушению соответствующих тканей и органов.
Образование клеток Гоше
Болезнь Гоше относится к подгруппе сфинголипидозов, то есть заболеваний, при которых не происходит переработки определенного вида липидов (жиров).
Болезнь Гоше — это самая распространенная разновидность ЛБН. Из-за генетической «поломки» в организме развивается недостаток фермента глюкоцереброзидазы. Он расщепляет сложные жиры глюкоцереброзиды, они же — гликосфинголипиды. В норме эти жиры входят в состав клеточных мембран, в частности, таких клеток крови, как лейкоциты и эритроциты. Когда эти клетки стареют, за их уничтожение берутся макрофаги, содержащие в себе множество лизосом. Глюкоцереброзидаза запускает процесс расщепления определенных компонентов клеточной мембраны на глюкозу и церамид.
Если же фермента не хватает, глюкоцереброзиды начинают накапливаться в лизосомах макрофагов, в результате чего образуются так называемые клетки Гоше. Их цитоплазма становится похожей на скомканный лист бумаги, а ядро оттесняется к периферии, так как клетка постепенно заполняется лизосоами, забитыми «под завязку» гликосфинголипидами. Последние токсичны для клеток.
В первую очередь страдают органы, где идет утилизация эритроцитов и лейкоцитов. К ним относятся селезенка, костный мозг, печень. По мере прогрессирования болезни к ним присоединяются кости, легкие, почки и др. Органы начинают увеличиваться в размерах, их работа нарушается. И хотя глюкоцереброзиды не накапливаются в нейронах, но они приводят к их деструкции и тем самым разрушительно влияют на нервную систему. Известно также, что на фоне болезни Гоше повышается вероятность развития гемобластозов — опухолей, в основе которых лежат кроветворные клетки.
Гены и болезнь Гоше
История болезни Гоше в медицине началась в 1882 году. Французский дерматолог Филипп Шарль Эрнест Гоше попутно работал гистологом — занимался изучением тканей, образцы которых он получал при вскрытии трупов. Его заинтересовала умершая женщина с увеличенной селезенкой. Изучив ткани органа, Гоше нашел патологически увеличенные клетки, которые впоследствии и получили его имя — клетки Гоше. Этот случай лег в основу его докторской диссертации и дал название самой болезни. В 1924 году немецкие врачи выделили из органов человека с болезнью Гоше жировое соединение, а еще через 10 лет стало понятно, что это глюкоцереброзид. Связь между накоплением данного вещества и дефицитом определенного фермента была установлена в 1965 году.
Сегодня известно, что ген, ответственный за выработку фермента глюкоцереброзидазы, расположен на 1-й хромосоме. Ученые нашли почти 200 участках гена, мутации на которых приводят к частичной или полной блокировке работы фермента, а также к уменьшению его срока жизни.
Болезнь Гоше наследуется по аутосомно-рецессивному типу. У человека 23 пары хромосом. Для проявления болезни надо, чтобы мутантный ген был на обеих хромосомах из пары. То есть, «звезды должны сойтись» именно так, чтобы у обоих родителей человека имелся мутантный ген. Сами они при этом остаются здоровыми людьми, так как вторая копия гена у них нормальная. Но их ребенок с 25%-ной вероятностью будет больным, а в 50% случаев — здоровым носителем одной копии мутантного гена. Болезнь встречается и у мужчин, и у женщин с одинаковой частотой.
Этносы и генетика: миф о «еврейской» болезни
Болезнь Гоше относится к орфанным (редким) заболеваниям. Это заболевание считается панэтническим, то есть выявляется у представителей самых разных национальностей. Но есть один нюанс. В среднем по миру болезнь Гоше встречается с частотой 1:40000 — 1:60000. То есть, только 1 из 40-60 тысяч человек родится с мутантными генами на обеих хромосомах из 1-ой пары. Гетерозиготное носительство, то есть когда мутантный ген есть только на одной хромосоме из пары и поэтому человек здоров — встречается в США с частотой 1 из 100-850 человек, это примерно 0,6% от всего населения страны.
У людей, носителей гена болезни Гоше на одной хромосоме, в 5 раз повышен риск развития болезни Паркинсона.
Но есть в мире этнос, где частота заболеваемости данным недугом выше в разы — это евреи-ашкенази, 1:450. Гетерозиготное носительство у них составляет 1:15, то есть 6% населения. Более того, по некоторым расчетам, 60% этой группы евреев имеют пару мутантных генов, то есть по сути более чем у половины из них есть болезнь Гоше. Но она у них практически никак не проявляется, либо симптомы ее слабо выражены.
Так что немудрено, что в свое время даже бытовало поверье, гласящее что болезнь Гоше имеет еврейские корни и вообще распространяется исключительно евреями (информация о группе ашкенази в этом мифе опускается). Но действительно, откуда же такая генетическая избирательность? Этот феномен объясняется очень просто. Традиции евреев-ашкенази таковы, что в их среде крайне распространены близкородственные браки. «Поломанные» гены не размываются среди миллиардов других геномов планеты, а на протяжении многих лет концентрируются внутри одной небольшой популяции. Собственно, болезнь Гоше — не единственное генетическое заболевание, которым эта группа населения болеет на порядок чаще, чем остальное население планеты.
Как проявляется болезнь Гоше?
На начальных этапах болезни наблюдается спленомегалия — увеличение селезенки в несколько раз. В тяжелых случаях аномально увеличенный орган по своим размерам превышает норму в 20 раз и достигает 15-20% от общего веса пациента.
Увеличивается также печень — в 1,5-2 раза, но в тяжелых случаях — до 10 раз. Анализы показывают, что количество глюкоцереброзида в тканях печени может быть превышено в 20-390 раз.
Огромная селезенка проявляет ненормальную активность и разрушает клетки крови. Поэтому параллельно у человека развивается анемия. Кроме того, по той же причине наблюдается еще и тромбоцитопения (дефицит тромбоцитов, которые необходимы для свертывания крови), поэтому пациент страдает от кровотечений разных видов: синяков на голенях, интенсивных менструаций, кровотечений из десен и из носа.
Патологии селезенки и печени не вызывают боли, но на фоне анемии развивается слабость.
Постепенно деформируются кости, приобретая характерный вид «колбы Эрленмейера». Именно скопления клеток Гоше в костях приводят к болям («костные кризы»), воспалению и повышают риски переломов.
Надо отметить, что болезнь Гоше по отдельным своим проявлениям похожа на многие другие заболевания. В то же время диагностируется она довольно просто: по анализу на фермент глюкоцереброзидазу в лейкоцитах.
Три формы болезни Гоше
Врачи говорят о существовании трех основных типов болезни Гоше.
I. Ненейронопатический тип.
Как следует из названия, при этой разновидности болезни Гоше нервная система не поражается. Это самый распространенный тип заболевания. Обычно первые симптомы проявляются в 30-40 лет. А вот каким образом — непредсказуемо. Спектр проявлений колеблется от тяжелых случаев с поражением костей и органов тела и до практически нормального состояния организма со слегка увеличенной селезенкой и хорошими показателями крови.
II. Острый нейронопатический тип.
При этой разновидности болезни развивается поражение головного мозга. Оно сопровождается обычно тяжелыми нарушениями работы других органов, косоглазием, повреждением скелета, гипертонусом мышц и т. п. Недуг проявляет себя очень рано — мало кто из детей доживает до двухлетнего возраста, обычно такие пациенты погибают от дыхательной недостаточности.
III. Хронический нейронопатический.
Тоже проявляется еще в детском возрасте, характеризуется разного рода нарушениями и неврологическими проблемами, но не столь выраженными и множественными, как у пациентов с болезнью II типа. Иногда такие люди страдают от слабоумия и эпилепсии.
Ученые предполагают, что при II и III формах болезни Гоше накопление глюкоцереброзида идет в немалой степени в головном мозге человека — отсюда такие обширные расстройства нервной системы.
Можно ли вылечить болезнь Гоше?
Вылечить — нет. Наука уже близка к генетической коррекции таких наследственных заболеваний, но эта проблема все-таки еще не решена.
До 1990-х годов болезнь Гоше лечили удалением увеличенной селезенки, что давало определенный эффект, но ненадолго. Кроме того, селезенка — это такой специальный орган для хранения «отходов» организма, которые нельзя переработать и вывести. Если его удалить, то «отходы» начинают откладываться в костях, печени и других неприспособленных для этого частях тела. Что ухудшает состояние человека. Так что можно сказать, что ранее терапия болезни Гоше была исключительно паллиативной.
Лишь четверть века назад удалось разработать эффективную ферментозаместительную терапию. В 1991 году американцы создали фермент альглюцеразу (Цередаза), а в 1994 году — препарат II поколения имиглицеразу (Церезим). Оба вещества являются синтезированными в лабораторных условиях аналогами глюкоцереброзидазы, причем даже улучшенными в том смысле, что «нацелены» на поступление именно в макрофаги.
Таким образом, сегодня в организм пациента вводится модифицированный фермент, который направляется прямо в органы-мишени, страдающие от болезни Гоше в первую очередь. Фермент долго в клетке существовать не может и быстро разрушается. Поэтому такая терапия должна проводиться на протяжении всей жизни пациента.
В России первые пациенты, проходящие ферментозаместительную терапию, появились в 1997 году. Бесплатным лечение для людей с болезнью Гоше в нашей стране стало только с 2006 года. С 2008 года болезнь Гоше входит в программу «7 нозологий» — и это дает возможность жить тем нашим соотечественникам, что получают ферментозаместительную терапию.
Лечение дорогостоящее: 40-65 тысяч за одну упаковку в зависимости от дозировки, и в месяц требуется не одна такая упаковка. Так что если человек не получает лекарство от государства — шансов у него практически нет. А ведь есть еще 6-7% пациентов с болезнью Гоше, у которых организм не приемлет Церезим — и это вызывает дополнительные сложности с их лечением.
Пока болезнь Гоше остается загадкой для врачей и ученых. Она может привести к смерти человека в первые 2 года жизни, а может быть случайно обнаружена в возрасте 70-80 лет, при том, что такой немолодой пациент никогда не испытывал проявлений болезни. Человечество еще не научилось лечить ее. Но генетическую диагностику может пройти любой человек — и пока это единственный способ профилактики болезни Гоше.
Источник

Болезнь Гоше – это генетическое заболевание, характеризующееся нарушением липидного обмена, недостаточностью лизосомальных ферментов, накоплением гликолипидов в клеточных структурах. Симптомы определяются типом патологии. Общими признаками являются увеличение печени, селезенки, снижение свертываемости крови. При I типе выявляются нарушения со стороны костной системы: остеопороз, частые переломы, инфекции костей. При II и III типе доминирует неврологическая симптоматика: судороги, паралич, косоглазие, задержка умственного развития. Диагностика основана на биохимическом анализе дефицитарного фермента. Лечение включает ферментозаместительную, субстратредуцирующую и симптоматическую терапию.
Общие сведения
Заболевание получило свое название по фамилии французского врача Филиппа Гоше. В 1882 году он описал симптомы и патанатомические особенности строения селезенки пациентки, которая умерла от сепсиса. Спустя несколько десятилетий при аналогичном клиническом случае Гоше определил накопление в селезенке глюкоцереброзида и недостаточность фермента глюкоцереброзидазы. Болезнь Гоше (сфинголипидоз, глюкозилцерамидный липидоз) относится к группе лизосомальных болезней накопления – наследственных патологий, при которых изменены функции клеточных органелл лизосом. Частота заболевания составляет от 1:40 тыс. до 1:70 тыс. Распространенность наиболее велика в сообществах, где допустимы браки между близкими родственниками, например, у евреев ашкенази. Носительство мутационного гена определяется примерно у 1 человека из 400.
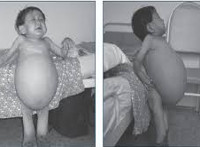
Болезнь Гоше
Причины
Глюкозилцерамидный сфинголипидоз является наиболее частой формой наследственных ферментопатий. Причиной его развития считается дефект гена GBA, который кодирует фермент лизосом бета-глюкозидазу (глюкоцереброзидазу), ответственную за расщепление липидов. Наследование болезни происходит аутосомно-рецессивным способом, для формирования ферментопатии необходимо присутствие пары измененных генов: один – от матери, другой – от отца. В супружеской паре, где оба родителя – носители мутации, вероятность рождения больного ребенка составляет 25%. Риск передачи одного дефектного гена, то есть риск носительства без развития болезни в таких семьях равен 50%. При наличии в генотипе двух мутантных аллелей функция глюкоцереброзидазы снижается на 15-30% от нормального уровня.
Патогенез
Патогенетической основой болезни является снижение каталитической активности бета-глюкозидазы. В результате нарушается процесс расщепления гликосфинголипидов (сложных соединений липидов и углеводов) до глюкозы и церамида. Аномально прогрессивное накопление макромолекул происходит в клетках, которые характеризуются повышенной скоростью их обновления – в макрофагах. Негидролизованные липиды концентрируются в лизосомах, образуются особые клетки накопления – клетки Гоше. Первичный метаболический сбой провоцирует вторичные расстройства биохимических процессов и клеточных функций. Из-за патологии жирового обмена развивается синдром активации макрофагов. Стимулируется моноцитопоэз, увеличивается содержание макрофагов в печени, селезенке, костном мозге. Это становится причиной спленомегалии, гепатомегалии, инфильтрации костного мозга. Расстройство регуляторной функции макрофагов является провоцирующим фактором цитопении, поражения костей и суставов.
Симптомы болезни Гоше
По возрасту дебюта и особенностям клинической картины выделяют три типа болезни. Первый тип наиболее распространен, имеет хронический характер течения. Симптомы чаще проявляются к 30-40 годам, реже болезнь манифестирует в детском возрасте. Увеличение размеров печени и селезенки начинается сразу после рождения, но клинически проявляется позже. Первыми признаками патологии становятся анемия, повышенная кровоточивость. Угнетение системы кроветворения сопровождается снижением уровня гемоглобина и тромбоцитов. Изменения со стороны опорно-двигательного аппарата представлены болями в костях и суставах, частыми переломами, деформациями (как правило, изменяется бедренная кость). У взрослых заметна гиперпигментация на лице и ногах: кожа темнеет, приобретает оттенок от желтоватого до желто-коричневого. Возможно появление плоских красных пятен с типичной локализацией в области вокруг глаз. Рост пациентов ниже среднего.
Второй тип болезни (острый инфантильный или острый нейропатический) встречается очень редко, развивается в промежутке от рождения до полутора лет, чаще всего симптомы дебютируют в первые три месяца жизни. Характеризуется стремительным течением, плохим откликом на лечение. На первый план выходят неврологические расстройства, спровоцированные скоплением клеток Гоше в центральной нервной системе. Дети слабо кричат, вяло сосут. Нарушен глотательный рефлекс, нередко отмечаются сбои цикла дыхания. Наблюдается заметная задержка психического и физического развития. На начальной стадии заболевания мышечный тонус снижен, через 9-12 месяцев после дебюта возникает гипертонус, особенно в мышцах шеи и конечностях. Развиваются судороги, косоглазие, спастический паралич. Печень и селезенка увеличены. Дети часто болеют тяжелой пневмонией.
Третий тип – ювенильный или подострый нейропатический. Первые признаки – увеличение селезенки и печени – возникают в 2-3 года. Полная симптоматика разворачивается в период с 6 до 15 лет. Клинические проявления поражения ЦНС включают гипертонус мышц, паралич спастического типа, косоглазие, непроизвольные спазмы, судороги, затрудненный цикл дыхания с трудностью вдоха, проблемы при глотании. Имеются расстройства психического развития: снижение интеллектуальных функций, несформированность речи и письма, эмоциональная неустойчивость, психозы. Дети отстают в половом развитии. Течение болезни неуклонно прогрессирующее.
Осложнения
Наиболее тяжелые осложнения выявляются при втором и третьем типе болезни. Поражение спинного и головного мозга приводит к нарушению дыхательного цикла, развиваются внезапные остановки дыхания, возрастает риск спазма гортани и смерти от удушья. Сниженный уровень тромбоцитов способен стать причиной обширных внутренних кровотечений. У больных с патологией первого типа распространенным осложнением является разрушение костей, их повышенная ломкость и инфекционные поражения. Ограничивается подвижность, пациенты не могут передвигаться самостоятельно, нуждаются в постороннем уходе.
Диагностика
Сбор анамнеза и физикальное обследование выполняется врачом-эндокринологом и неврологом, дополнительно назначаются консультации генетика, гематолога, офтальмолога, педиатра, психиатра. Анамнестические данные включают наличие болезни Гоше у родственников. При осмотре выявляются типичные признаки: низкий рост, патологии костей, неврологические симптомы (косоглазие, атаксия, паралич), геморрагический синдром, гиперпигментация кожи. Иногда подозрение на заболевание возникает после случайного выявления увеличенной селезенки на снимках УЗИ, угнетении кроветворной системы по данным общего анализа крови. Для подтверждения диагноза, исключения других метаболических наследственных патологий, остеомиелита, костного туберкулеза, вирусного гепатита и онкологических поражений крови проводится специфическая диагностика:
- Клиническое, биохимическое исследование крови. У большинства больных определяется тромбоцитопения, лейкопения, анемия, которая у детей обычно имеет железодефицитное происхождение. В результатах биохимического анализа обнаруживается сниженная активность глюкоцереброзидазы.
- Ферментный анализ клеток. При болезни Гоше в образцах сухой крови и в фибробластах кожи выявляется недостаточная активность глюкозидазы. Степень дефицитарности фермента не имеет прямой корреляции с выраженностью симптомов. Дополнительный биохимический маркер – хитотриозидаза. Этот фермент синтезируется активированными макрофагами, характерно повышение его активности в 6-10 раз.
- Морфологическое изучение костного мозга. Подтверждается наличие специфических для данного заболевания структур – клеток Гоше. Результат позволяет исключить гемобластоз и лимфопролиферативное заболевание.
- Исследование структуры костной ткани. С целью оценки тяжести поражения костно-суставной системы выполняется денситометрия, рентгенография и/или МРТ костей скелета. Возможен диффузный остеопороз, могут визуализироваться колбы Эрленмейера, очаги остеолизиса, остеосклероза и остеонекроза. На ранних стадиях болезни отмечается остеопения, инфильтрация костного мозга.
- Визуализирующее исследование селезенки, печени. Проводится УЗИ и МРТ внутренних органов. По результатам устанавливается наличие или отсутствие очаговых поражений, измеряется объем увеличенного органа. Исходные показатели в последующем позволяют контролировать эффективность терапии.
- Молекулярно-генетические исследования. ДНК-диагностика является необязательной процедурой. Подтверждение мутации в гене GBA бывает необходимо при неоднозначности биохимических исследований, а также в рамках пренатальных и преимплантационных обследований.
Лечение болезни Гоше
Специализированная помощь больным с первым и третьим типом болезни направлена на устранение симптомов и компенсацию первичного генетического дефекта – увеличение количества недостающего фермента, усиление катаболизма гликосфинголипидов. При 2 типе патологии терапевтические мероприятия оказываются недостаточно эффективными, усилия врачей сводятся к облегчению клинических проявлений – болей, судорог, дыхательных расстройств. Общая схема включает следующие направления:
- Ферментозаместительная терапия. Основным методом лечения является пожизненная ферментная заместительная терапия (ФЗТ) с применением рекомбинантной глюкоцереброзидазы. Эффективность достаточно высока – симптомы полностью купируются, качество жизни больных повышается. ФЗТ целесообразна при третьем и первом типе заболевания. Препараты вводятся внутривенно. Частые инфузии иногда становятся причиной воспалительных заболеваний вен (флебитов).
- Субстрат-редуцирующая терапия. Данное направление является новым в лечении болезни Гоше, относительно широко распространено в США и странах Европы. Нацелено на снижение скорости производства субстрата гликосфинголипидов и ускорение катаболизма накапливающихся макромолекул. В качестве препаратов выступают специфические ингибиторы глюкозилцерамидсинтазы. Метод показан при заболевании 1 типа с легкими и умеренными симптомами.
- Симптоматическая терапия. При явлениях остеопороза назначается комплексная терапия, включающая прием кальцийсодержащих препаратов, витамина D и соблюдение диеты, обогащенной кальцием. Эти меры позволяют замедлить потерю костной массы, повысить прочность костей, предотвратить переломы. При скелетных осложнениях применяются анальгезирующие средства (НПВС), антибактериальная терапия. Симптомы неврологических нарушений купируются противоэпилептическими препаратами, ноотропами, миорелаксантами.
Прогноз и профилактика
Благоприятный исход наиболее вероятен у пациентов с 1 типом заболевания – комплексный терапевтический подход позволяет нормализовать функциональность глюкоцереброзидазы, предупредить развитие осложнений, избежать инвалидизации. При 3 типе прогноз зависит от характера течения болезни, индивидуальной реакции организма на лечебные мероприятия. 2 тип имеет крайне тяжелые проявления и завершается гибелью больного. Профилактика проводится во время планирования беременности и на ее начальных сроках. Медико-генетическое консультирование рекомендуется семьям, имеющим близких родственников с данной патологией. При высоком риске передачи мутации будущему ребенку в первом триместре выполняется исследование уровня фермента в амниотической жидкости, решается вопрос о прерывании беременности.
Источник
