Глобальная инициатива по хронической обструктивной болезни легких gold

 Хроническая обструктивная болезнь легких (ХОБЛ) относится к наиболее распространенным заболеваниям человека, что обусловлено загрязнением окружающей среды, табакокурением и повторяющимися респираторными инфекционными заболеваниями.
Хроническая обструктивная болезнь легких (ХОБЛ) относится к наиболее распространенным заболеваниям человека, что обусловлено загрязнением окружающей среды, табакокурением и повторяющимися респираторными инфекционными заболеваниями.
Во многих странах отмечается устойчивая тенденция к увеличению распространенности ХОБЛ. По оценкам экспертов, около 10 % людей в возрасте старше 40 лет имеют ограничение скорости воздушного потока соответствующее второй степени тяжести ХОБЛ и около 25% — первой. По данным Европейского респираторного общества только 25% случаев заболевания выявляется на ранних стадиях.
Для того чтобы привлечь большее внимание к проблеме ХОБЛ, ее лечению и профилактике, в 1998 г. инициативная группа ученых убедила Национальный институт сердца, легких и крови (США) и ВОЗ сформировать «Глобальную инициативу по хронической обструктивной болезни легких» (GOLD – Global Initiative for Chronic Obstructive Lung Disease). Первым шагом в программе GOLD была подготовка согласительного доклада рабочей группы «Глобальная стратегия диагностики, лечения и профилактики ХОБЛ», опубликованного в 2001 году. Этот документ вобрал в себя последние научные изыскания, результаты многочисленных клинических испытаний препаратов, новые приемы в ведении больных ХОБЛ. Но медицинская наука не стоит на месте, поэтому «Глобальная стратегия по диагностике, лечению и профилактике ХОБЛ» периодически пересматривается. 23 января 2014 года издана новая версия доклада рабочей группы международной программы GOLD 2014 года.
Хроническая обструктивная болезнь легких – заболевание, которое можно предотвратить и лечить, характеризующееся персистирующим ограничением скорости воздушного потока, которое обычно прогрессирует и связано с повышенным хроническим воспалительным ответом легких на действие патогенных частиц или газов. У ряда пациентов обострения и сопутствующие заболевания могут влиять на общую тяжесть ХОБЛ.
ХОБЛ является примером мультифакторного заболевания, в развитии которого наряду с генетическими факторами ведущая роль принадлежит курению и воздействию аэрополлютантов (промышленных и бытовых). Курение считается главным агрессивным экзогенным фактором, который инициирует целый комплекс дисфункций дыхательной системы. При сочетании курения с конституционными и наследственными факторами риска вероятность возникновения ХОБЛ существенно возрастает. Загрязнение окружающей среды большим количеством токсичных веществ способствует снижению барьерной функции слизистой оболочки дыхательных путей, вызывает респираторные дисфункции и нарушает механизмы иммунной защиты. В основе патогенеза лежит воспалительная реакция, которая ведет вначале к частично обратимому, а в дальнейшем необратимому нарушению бронхиальной проходимости и ограничению скорости воздушного потока. Болезнь отличается неуклонно прогрессирующим характером и выраженными системными эффектами, которые могут усугублять ее течение.
Диагноз ХОБЛ основывается на клинических симптомах (одышка, хронический кашель с отделением мокроты или без нее), наличия в анамнезе характерных факторов риска и при условии обязательной верификации методом спирометрии, во время которой отмечают снижение соотношения ОФВ1/ФЖЕЛ менее 0,70.
Таблица 1. Классификация ХОБЛ в соответствии со степенью тяжести (основанная на постбронходилатационном ОФВ1)
| Степень по GOLD | ОФВ1, % от должного |
| I — легкая | ≥80 |
| II — умеренная | ≥50 и <80 |
| III — тяжелая | ≥30 и <50 |
| IV — крайне тяжелая | <30 или ОФВ1 <50% от должных величин в сочетании с хронической дыхательной недостаточностью |
Классификация степени тяжести бронхообструкции у пациентов с ХОБЛ не изменилась, оценивается по ОФВ1 (табл.1). Несмотря на то, что исследование легочной функции, в частности определение ОФВ1, является важным инструментом в оценке и классификации ХОБЛ, этот показатель не дает полного представления о тяжести течения и скорости прогрессирования заболевания и слабо коррелирует с такими важными характеристиками ХОБЛ, как одышка по шкале mMRC, статус здоровья по респираторному вопроснику SGRQ, результатами теста с 6-минутной ходьбой и количество обострений. Всё вышеперечисленное определило современную концепцию интегральной оценки тяжести ХОБЛ.
Таблица 2. Модифицированная шкала одышки Medical Reseach Council Dyspnea Scale
| Степень | Тяжесть | Описание |
| Нет | Одышка только при интенсивной физической нагрузке | |
| 1 | Легкая | Одышка при быстрой ходьбе, небольшом подъеме |
| 2 | Средняя | Одышка заставляет идти медленнее, чем люди того же возраста |
| 3 | Тяжелая | Одышка заставляет останавливаться при ходьбе примерно через каждые 100 метров |
| 4 | Очень тяжелая | Одышка не позволяет выйти за пределы дома или проявляется при одевании |
Для количественной оценки степени тяжести одышки применяют модифицированную шкалу одышки Medical Research Council Dyspnea Scale (mMRC) (табл. 2). Также для оценки степени влияния ХОБЛ на самочувствие и повседневную жизнь пациентов применяют тест оценки ХОБЛ — CAT (COPD Assessment Test), который отражает общее видение болезни врачами и пациентами. Вопросник состоит из 8 пунктов по оценке нарушения состояния здоровья при ХОБЛ. Пункты сформированы по 6-балльной семантической дифференциальной шкале от 0 до 5 баллов. Наибольшее суммарное количество баллов – 40 – говорит о том, что болезнь проявляется максимальными симптомами и оказывает выраженное влияние на жизнь пациента.
Опросник CAT (COPD Assessment Test)

Комплексная оценка состояния пациента с ХОБЛ основывается на степени выраженности симптомов, риске развития обострений в будущем, тяжести бронхообструкции по данным спирометрии, а также идентификации сопутствующих заболеваний. При этом учитывают данные по mMRC, CAT и степень тяжести бронхообструкции по GOLD, что позволяет разделить пациентов на 4 группы — от A до D с указанием риска возникновения неблагоприятных событий (обострений, госпитализаций из-за обострений ХОБЛ, смерти) в будущем (рис. 1):
- пациенты группы А – «низкий риск», «меньше симптомов». Обычно у таких пациентов наблюдается спирометрический класс GOLD 1 или GOLD 2 (ограничение скорости воздушного потока легкой или средней степени тяжести) и/или 0–1 обострение в год и степень 0–1 по mMRC или <10 баллов по CAT;
- пациенты группы В – «низкий риск», «больше симптомов». Обычно у таких пациентов наблюдается спирометрический класс GOLD 1 или GOLD 2 и/или 0–1 обострение в год и степень ≥2 по mMRC или ≥10 баллов по CAT;
- пациенты группы С – «высокий риск», «меньше симптомов». Обычно у таких пациентов наблюдается спирометрический класс GOLD 3 или GOLD 4 (ограничение скорости воздушного потока тяжелой или крайне тяжелой степени) и/или ≥2 обострений в год или ≥ 1 обострения, потребовавшего госпитализации, и степень 0–1 по mMRC или <10 баллов по CAT;
- пациенты группы D – «высокий риск», «больше симптомов». Обычно у таких пациентов наблюдается спирометрический класс GOLD 3 или GOLD 4 и/или ≥2 обострений в год или ≥ 1 обострения, потребовавшего госпитализации, и степень ≥2 по mMRC или ≥10 баллов по CAT.

При использовании подхода, представленного на рис. 1, сначала нужно оценить симптомы заболевания по шкале mMRC или CAT и определить, относится ли пациент к левой стороне квадрата – «меньше симптомов» (степень 0–1 по mMRC или <10 баллов по CAT) или к правой стороне – «больше симптомов» (степень ≥2 по mMRC или ≥10 баллов по CAT). Затем следует оценить риск обострений, чтобы определить, относится ли пациент к нижней части квадрата «низкий риск» или к верхней части – «высокий риск». Это можно сделать одним из двух методов: 1) использовать спирометрию для определения степени тяжести ограничения скорости воздушного потока согласно классификации GOLD (классы GOLD 1 и GOLD 2 указывают на низкий риск обострений, а GOLD 3 и GOLD 4 – на высокий риск); 2) определить количество обострений, которые были у пациента за предшествующие 12 месяцев (0 или 1 без госпитализации указывают на низкий риск обострений, 2 и более или более 1 с госпитализацией – на высокий риск). У некоторых пациентов уровни риска, оцененные по этим двум методикам, не совпадают; в таком случае уровень риска следует определять методом, указывающим на высокий риск обострений.
Важным нововведением последних редакций GOLD стало то, что в основу разделения пациентов на группы и, следовательно, выбора для них схемы терапии была положена не только степень нарушения функции легких по данным спирометрии (показатель ОФВ1), как это было ранее, но и другие важные параметры — выраженность симптомов болезни и частота обострений в анамнезе. В новой редакции GOLD 2014 года в отличие от предыдущих версий изменена интегральная оценка ХОБЛ. Пациенты, у которых есть хотя одно обострение в течение года, приведшее к госпитализации, относятся к группам высокого риска (C, D) и требуют более пристального внимания. Учитывая, что в наших условиях госпитализация иногда осуществляется по парамедицинским (социальным) показаниям, необходимо оценивать при сборе анамнеза для интегральной оценки тяжести тяжесть обострения (была ли необходимость госпитализации).
Немедикаментозное лечение предполагает обязательный отказ от курения, проведение легочной реабилитации (для пациентов групп B, C и D), повышение уровня физической активности и проведение вакцинации против гриппа и пневмококковой инфекции. Кроме того, применяют оксигенотерапию и вентиляционную поддержку, а также хирургические методы лечения (операции по уменьшению объема легких и буллэктомия у пациентов с преимущественно верхнедолевой эмфиземой легких и сниженной переносимостью физической нагрузки) при наличии показаний.
Таблица 3. Фармакотерапия стабильной ХОБЛ
Категория пациентов | Препараты | ||
| первого ряда | альтернативные | другое возможное лечение* | |
| A | КДАХ или КДБА по требованию | ДДАХ или ДДБА или КДБА и КДАХ | Теофиллин |
| B | ДДАХ или ДДБА | ДДАХ и ДБА | КДБА и/или КДАХ Теофиллин |
| C | ИГКС + ДДБА или ДДАХ | ДДАХ и ДДБА или ДДАХ и ингибиторы ФДЭ-4 или ДДБА и ингибиторы ФДЭ-4 | КДБА и/или КДАХ Теофиллин |
| D | ИГКС + ДДБА и/или ДДАХ | ИГКС + ДДБА и ДДАХ, или ИГКС+ДДБА и ингибиторы ФДЭ-4, или ДДАХ и ДДБА, или ДДАХ и ингибиторы ФДЭ-4 | Карбоцистеин КДБА и/или КДАХ Теофиллин |
Примечание. КДАХ — короткодействующий антихолинергический препарат, КДБА — короткодействующий бетта 2-агонист, ДДАХ — длительнодействующий антихолинэргический препарат, ДДБА — длительнодействующий бетта 2-агонист, ИГКС — ингаляционные глюкокортикостероиды, ФДЭ — фосфодиэстераза;
*-препараты в данном столбце могут быть использованы сами по себе или в комбинации с другими препаратами первого или второго столбцов.
В новой редакции GOLD предлагается модель назначения фармакотерапии в соответствии с индивидуализированной оценкой симптомов и риска обострения представлена в табл. 3. Препараты в каждой ячейке данной таблицы приведены в алфавитном порядке.
В соответствии с новой редакцией GOLD фармакотерапия ХОБЛ направлена главным образом на уменьшение выраженности симптоматики, снижение частоты и тяжести обострений и улучшение статуса здоровья и переносимости физической нагрузки.
Литература
1. Decramer, M., Janssens W., Miravitlles M. Chronic ob- structive pulmonary disease. Lancet. 2012; 1341-1351.
2. Глобальная стратегия: диагностика, лечение и профи- лактика хронической обструктивной болезни легких// До- клад рабочей группы Национального Института Сердца, Лег- ких и Крови и Всемирной организации Здравоохранения. – 2014.
Авторы статьи: А.А. Королева, Ю.Л. Журавков, С.М. Метельский
Кафедра военно-полевой терапии ВМедФ в УО “БГМУ”, ГУ “432 ГВКМЦ”
Источник
В статье представлен алгоритм диагностики и терапии хронической обструктивной болезни легких
Цель публикации: представить индикаторы качества оказания медицинской помощи при хронической обструктивной болезни легких (ХОБЛ) и алгоритм ранней диагностики и лечения для практического врача.
В соответствии с последними декларативными документами, посвященными ХОБЛ, задачами лечения этого заболевания при стабильном течении являются [1, 2]:
А. Снижение выраженности симптомов болезни, включающее:
• устранение или уменьшение жалоб;
• улучшение переносимости физических нагрузок;
• улучшение состояния здоровья.
Б. Снижение риска прогрессирования ХОБЛ:
• предотвращение прогрессирования заболевания;
• предотвращение и лечение обострений;
• предотвращение смертельных исходов.
Согласно Global Initiative for Chronic Obstructive Pulmonary Disease (GOLD 2016) особое внимание обращается на уменьшение клинической симптоматики, улучшение качества жизни (КЖ) при минимальных побочных эффектах от лечения [1]. Действительно, наиболее частым поводом для первого обращения к врачу-терапевту больного с предполагаемым диагнозом ХОБЛ является появление новых жалоб или усиление знакомых пациенту симптомов, таких как увеличение отделения мокроты, появление (усиление) гнойной мокроты, увеличение одышки, которые нередко сопровождаются повышением температуры тела [3]. Установлено, что пациенты с симптомами, проявляющимися независимо от времени суток, имеют худший прогноз и более низкое КЖ (общее самочувствие, депрессия, тревожность, качество сна) [4].
В каждом клиническом фенотипе и при каждой степени тяжести ХОБЛ (от легкой до крайне тяжелой) имеются пациенты с различной степенью выраженности симптомов, которые оказывают существенное влияние на течение ХОБЛ, являясь предикторами обострений заболевания. Следовательно, основными задачами, стоящими перед лечащим врачом, являются адекватное влияние на симптомы заболевания и предотвращение обострений ХОБЛ. О значении выраженности симптомов ХОБЛ свидетельствуют сравнительные исследования по оценке выживаемости больных ХОБЛ в соответствии с подгруппами 1–4 (по GOLD 2007) и A–D (по GOLD 2011) (рис. 1) [5]. Из представленных данных следует, что выживаемость при ХОБЛ хуже в группе B, чем в группе C, т. е. у больных с выраженными симптомами, несмотря на удовлетворительные показатели объема форсированного выдоха за 1-ю секунду (ОФВ1) (≥50% от должной величины), по сравнению с пациентами с невыраженными симптомами, но с низкими показателями ОФВ1 (<50% от должной величины).
![Рис. 1. Выживаемость в группах ХОБЛ 1–4 и A–D (по GOLD 2007 и GOLD 2011) [5] Рис. 1. Выживаемость в группах ХОБЛ 1–4 и A–D (по GOLD 2007 и GOLD 2011) [5]](https://www.rmj.ru/upload/medialibrary/050/0506a51d3e51ee7a772ccfe6d0373e40.png)
Контроль симптомов заболевания помогает лучше оценить состояние пациента, ответ на лечение, обеспечить предупреждение обострений и замедлить прогрессирование и достичь контроля ХОБЛ [6].
Возможен ли контроль при ХОБЛ? Понятие «контроль ХОБЛ» включает поддержание состояния пациента с минимальным влиянием заболевания на повседневную активность (принимая во внимание тяжесть течения ХОБЛ). Оптимальный контроль ХОБЛ может быть определен следующими критериями [7]:
• минимальное воздействие ХОБЛ на человека в соответствии с исходной тяжестью заболевания (симптомы заболевания не выражены);
• стабильность состояния, т. е. отсутствие значимого клинического ухудшения и отсутствие обострений в течение по крайней мере последних 3-х месяцев.
Достижение контроля над заболеванием зависит от выполнения критериев качества оказания медицинской помощи пациенту с ХОБЛ. На основании рекомендаций Министерства здравоохранения РФ в 2016 г. совместно с профессором Айсановым З.Р. (ФГБУ «НИИ пульмонологии» ФМБА России) разработаны критерии оценки качества оказания медицинской помощи при ХОБЛ (табл. 1).

Соблюдение критериев качества медицинской помощи больным с ХОБЛ, отражающих анамнестические сведения, симптомы болезни, функциональные показатели, своевременность и адекватность лечебных мероприятий при стабильном течении заболевания и при обострении в значительной мере поможет в достижении контроля ХОБЛ. Таким образом, целью соблюдения критериев качества при ХОБЛ является достижение контроля над болезнью, которое для лечащего врача заключается в проведении диагностических, лечебных и профилактических мероприятий.
Известно, насколько актуальным является значение ранней диагностики ХОБЛ и назначение своевременной адекватной стартовой терапии. По данным Европейского респираторного общества, только 25% случаев заболевания диагностируются своевременно [8]. В помощь врачу первичного звена (терапевта) представляем алгоритм ранней диагностики ХОБЛ (табл. 2), показания и необходимый объем обследований для направления на консультацию к пульмонологу.
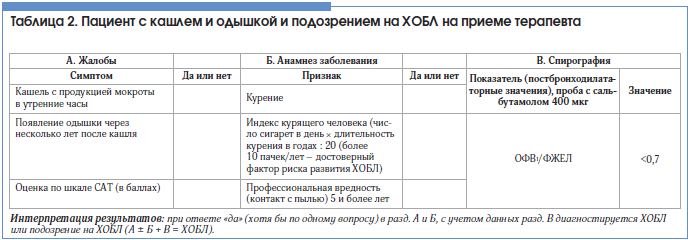
Показаниями для направления к пульмонологу являются:
• подозрение или впервые диагностированная ХОБЛ;
• дифференциальная диагностика ХОБЛ;
• отсутствие эффекта от лечения или нежелательные явления от назначенной лекарственной терапии.
Для направления на консультацию пульмонолога необходимо представить данные обследования:
• выписку из амбулаторной карты или истории болезни;
• анализ крови с лейкоцитарной формулой;
• ОФВ1 и результат ингаляционного бронхолитического теста с сальбутамолом 400 мкг (у больного вне обострения заболевания);
• рентгенография органов грудной клетки (ОГК) в 2-х проекциях;
• компьютерная томография (КТ) органов грудной клетки (при возможности);
• электрокардиография;
• эхокардиография (при необходимости).
В соответствии с GOLD и Федеральными клиническими рекомендациями по диагностике и лечению хронической обструктивной болезни легких 2014 г. для всех пациентов независимо от тяжести заболевания рекомендуются нефармакологические методы воздействия на ХОБЛ и медикаментозная терапия [1, 2].
Характеризуя нефармакологические методы воздействия на ХОБЛ, необходимо подчеркнуть, что они являются неотъемлемой и весьма значимой частью лечения, профилактики обострений и прогрессирования заболевания (табл. 3).

Курение – безусловный фактор развития ХОБЛ и ее более быстрого прогрессирования [9]. Среди механизмов снижения показателей функции внешнего дыхания у курящих рассматривается дефицит витамина D, который обладает иммуномодулирующими и противовоспалительными эффектами, подавляемыми действием сигаретного дыма. В 20-летнем исследовании продемонстрировано, что функция легких у курящих лиц с недостатком витамина D снижается быстрее, чем у лиц с нормальным уровнем содержания витамина D [10]. В другом исследовании показано высокое распространение дефицита витамина D – 66% в популяции курящих, страдающих ХОБЛ [11]. Прекращение курения приводит к замедлению падения ОФВ1 почти в 2 раза по сравнению с теми пациентами, которые продолжали курить, что было установлено в 5-летнем исследовании здоровья легких у 5887 больных ХОБЛ легкой и умеренной степени тяжести (Lung Health Study – LHS) [9]. Отказ от курения является единственной мерой, предупреждающей прогрессирование развития эмфиземы и приводящей к улучшению респираторных симптомов [12]. Вакцинация против гриппа и пневмококковой инфекции должны быть предложены каждому пациенту с ХОБЛ. Вакцинопрофилактика более эффективна у пациентов пожилого возраста и лиц с более тяжелым течением заболевания или сердечной сопутствующей патологией, т. к. именно эта категория больных ХОБЛ имеет наибольшую вероятность развития обострений основного заболевания или тяжелой сопутствующей патологии. Недостаточное внимание практикующими врачами уделяется легочной реабилитации, включающей в себя, помимо физических тренировок, образовательные и психосоциальные программы, созданные для улучшения физического и эмоционального состояния больных и обеспечения длительной приверженности пациента поведению, направленному на сохранение здоровья [2].
В GOLD последних лет и в Федеральной программе по ХОБЛ медикаментозная терапия представлена различным ассортиментом лекарственных препаратов, распределенных на 4 группы (А, В, С, D) в соответствии с тяжестью ХОБЛ, выраженностью симптомов и частотой обострений заболевания [1, 2]. Каждая группа включает несколько лекарственных препаратов и их сочетаний.
В настоящее время длительно действующие бронходилататоры (ДДБД), имеющие высокий уровень эффективности и безопасности, являются основными лекарственными препаратами (препаратами 1-й линии) для базисной (регулярной) терапии больных ХОБЛ [1, 2]. Эта группа лекарственных средств назначается всем больным ХОБЛ независимо от тяжести заболевания. Доказано, что двойная бронходилатация (длительно действующие антихолинергические (ДДАХ) препараты и длительно действующие β2–агонисты (ДДБА)) является предпочтительней по сравнению с монотерапией каждым из препаратов у больных с выраженными симптомами и приоритетной для стартовой терапии ХОБЛ [13–17]. В недавно опубликованном решении совета экспертов Российского респираторного общества о целесообразности применения фиксированных комбинаций ДДАХ и ДДБА в фармакотерапии ХОБЛ подчеркивается их важнейшая роль по влиянию на редукцию симптомов, улучшению легочной функции, переносимости физической нагрузки и КЖ, предотвращению обострений заболевания [18].
В связи с появлением новых ДДАХ и фиксированных комбинаций ДДАХ/ДДБД, зарегистрированных в Российской Федерации, представляет интерес оценка их эффективности с точки зрения уровня доказательности и силы рекомендаций (табл. 4). В таблице дана характеристика медикаментозной терапии больных ХОБЛ стабильного течения, где представлены данные по эффективности новых бронходилататоров длительного действия и их фиксированных комбинаций в соответствии с уровнями доказательности и силой рекомендаций (табл. 5 и 6). Таблица составлена на основании Кохрановских обзоров, метаанализов, рандомизированных контролируемых исследований и дополняет данные о лекарственных средствах, нашедших отражение в Федеральных клинических рекомендациях по диагностике и лечению ХОБЛ 2014 г. [2].
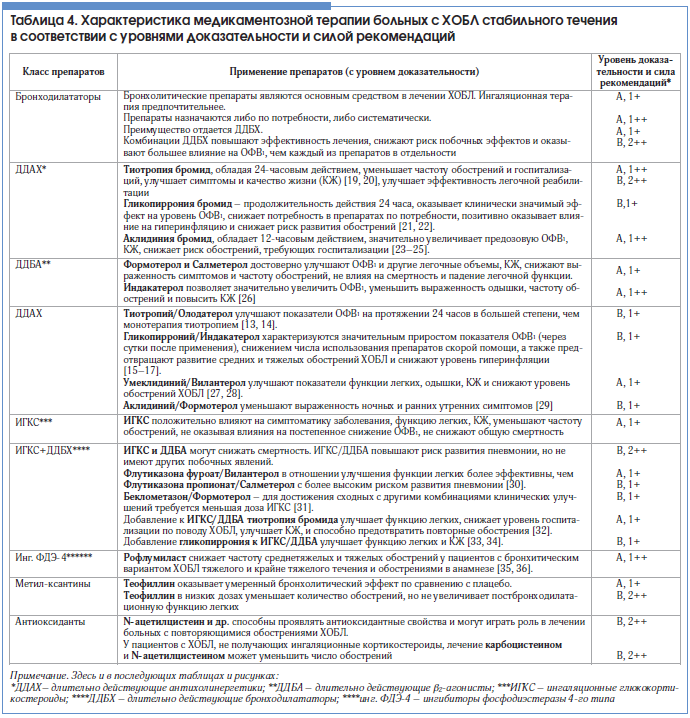


Ингаляционные глюкокортикостероиды (ИГКС) в комбинации с ДДБА или в составе «тройной» комбинации с ДДАХ рекомендуются для длительного лечения ХОБЛ при наличии частых обострений в анамнезе [1, 2]. В то же время данные о влиянии ИГКС-содержащих режимов терапии ХОБЛ на смертность ограничены и противоречивы, кроме того, комбинированная терапия ИГКС+ДДБА повышает риск развития пневмонии, в связи с чем включение ИГКС в терапию ХОБЛ требует более детальной оценки клинической картины заболевания [34].
Ингибиторы фосфодиэстеразы 4-го типа (инг. ФДЭ-4) в комбинации с ДДАХ или в составе «тройной» комбинации с ИГКС/ДДБА, согласно рекомендациям GOLD, показаны больным ХОБЛ в группах С и D. В исследовании REACT по изучению (ИГКС/ДДБА)+ДДАХ+ФДЭ-4 было показано достоверное снижение риска тяжелых обострений, приведших к госпитализации [35]. С формальной точки зрения в рекомендациях GOLD инг. ФДЭ-4, также как и ИГКС, могут быть назначены больным с частыми обострениями, в то же время доказано и достаточно хорошо известно, что инг. ФДЭ-4 (рофлумиласт) снижают частоту среднетяжелых и тяжелых обострений у пациентов с бронхитическим вариантом ХОБЛ тяжелого и крайне тяжелого течения и обострениями в анамнезе (А, 1++) [36].
Одним из основных вопросов, стоящих перед лечащим врачом, является определение объема стартовой и последующей терапии больным ХОБЛ. К сожалению, распределение больных в соответствии с современной классификацией GOLD на 4 группы (A, B, C, D) не дает конкретного ответа на этот вопрос [1, 2]. Несмотря на то что выбор лекарственной терапии, на основании классификации GOLD, зависит от выраженности симптомов, степени ограничения воздушного потока и риска обострений, перед врачом стоит непростая задача конкретного выбора той или иной схемы лекарственной терапии для больного ХОБЛ.
Для оптимизации базисной терапии ХОБЛ, и в частности решения вопроса о назначении ИГКС или инг. ФДЭ-4, целесообразно рассматривать известные фенотипы (бронхитический, эмфизематозный, оverlap-фенотип – сочетание ХОБЛ и бронхиальной астмы (БА)) дополнительно с точки зрения особенностей клеточного характера воспаления, а также с учетом методов лучевой диагностики (компьютерно-томографическая фенотипическая характеристика), анамнестических сведений о характере обострений (инфекционное, неинфекционное, пневмонии в анамнезе).
Указание в анамнезе на перенесенные пневмонии у больных ХОБЛ расценивается как противопоказание для назначения ИГКС, хотя механизм пневмонии у больных ХОБЛ на фоне лечения ИГКС окончательно не выяснен. Рассматривая причины развития пневмонии при лечении ИГКС, следует учитывать, что разные ИГКС проявляют разную иммуносупрессивную активность (например, иммуносупрессивная активность флутиказона пропионата в 10 раз выше по сравнению с будесонидом) [37]. В свою очередь, КТ-фенотипическая характеристика помогает понять клиническое разнообразие ХОБЛ. Например, КТ высокого разрешения у больных ХОБЛ III–IV по GOLD позволили выявить бронхоэктазию у 33,8% из них [38]. В этой связи наличие именно инфицированной бронхоэктазии, а не только наличие бронхоэктазов у больных ХОБЛ следует рассматривать как фактор риска инфекционного обострения на фоне лечения ИГКС.
К настоящему времени имеется достаточно оснований для рекомендации включения ИГКС + ДДБА в схему терапии ХОБЛ с учетом уровня эозинофилов в анализах мокроты, периферической крови или уровня FeNO. Потенциальными маркерами назначения ИГКС в сочетании с ДДБА являются: число эозинофилов в мокроте ≥3%, в периферической крови ≥300 кл/мл или увеличение показателей FeNO≥25 ppb, хотя эти значения не всегда являются абсолютными показаниями к назначению указанных препаратов при ХОБЛ [39].
Следовательно, при решении вопроса о включении ИГКС в терапию ХОБЛ у больных с частыми обострениями рекомендуется взвешивать риск и пользу от назначения ИГКС, выделять отдельные группы/подгруппы пациентов с учетом данных КТ высокого разрешения, клеточного характера воспаления, анамнестических сведений на основании медицинской документации о характере обострений заболевания (инфекционное, неинфекционное). Эти подходы в решении вопроса о назначении ИГКС относятся, прежде всего, к больным с бронхитическим фенотипом ХОБЛ. Выделение различных вариантов бронхитического фенотипа (подгрупп) помогут врачу выбрать оптимальный вариант медикаментозной терапии.
Что касается эмфизематозного фенотипа ХОБЛ, то для этой категории больных препаратами выбора являются ДДБД, а при терминальном течении – хирургическая редукция легочных объемов, длительная кислородотерапия на дому, трансплантация легких. Доказательств целесообразности назначения ИГКС или инг. ФДЭ-4 пациентам с эмфизематозным фенотипом в настоящее время не получено.
Место ИГКС у больных с сочетанием ХОБЛ и БА определено на основании международных и национальных руководств, в согласованных рекомендациях экспертного совета Российского респираторного общества [40].
В таблице 7 представлены схемы базисной (регулярной) медикаментозной терапии ХОБЛ с учетом выраженности симптомов и фенотипов ХОБЛ (бронхитический, эмфизематозный, overlap-фенотип – сочетание ХОБЛ и БА), а также особенностей феноэндотипической картины бронхитического варианта ХОБЛ.
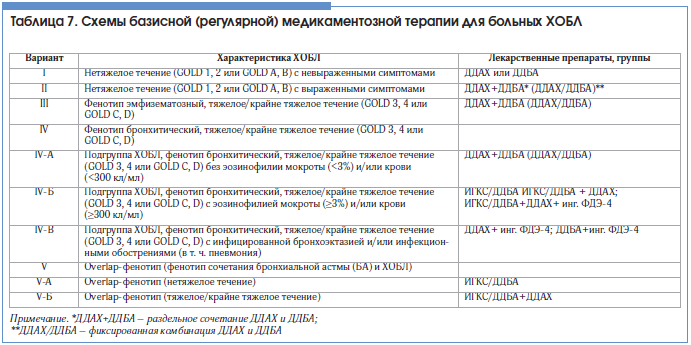
На основании представленных схем лечения базисной (регулярной) медикаментозной терапии ХОБЛ вниманию читателя представляется алгоритм поэтапной терапии для пациентов с установленным диагнозом ХОБЛ (рис. 2).

Заключение
Таким образом, в данной статье вниманию врача первичного звена (терапевта) представлены алгоритм ранней диагностики ХОБЛ, показания для направления на консультацию к пульмонологу, индикаторы качества оказания медицинской помощи больным ХОБЛ и схемы поэтапной базисной стартовой терапии, составленные с учетом уровня доказательности и силы рекомендаций. Авторы выражают уверенность, что изложенный материал поможет врачу-интернисту в ранней диагностике и оказании помощи больным столь тяжелым заболеванием.
Источник
