Болезни с аутосомно доминантным типом наследования

Чаще всего патологии передает тип наследования аутосомно-доминантный. Это моногенное наследование одного из признаков. Помимо этого, болезни могут передаваться детям аутосомно-рецессивным и аутосомно-доминантным типом наследования, а также по митохондриальному признаку.

Типы наследования
Моногенное наследование гена может быть рецессивным и доминантным, митохондриальным, аутосомным или сцепленным с половыми хромосомами. При скрещивании может получиться потомство с самыми разными типами признаков:
- аутосомно-рецессивными;
- аутосомно-доминантными;
- митохондриальными;
- Х-доминантное сцепление;
- Х-рецессивное сцепление;
- У-сцепление.
Разные типы наследования признаков — аутосомно-доминантный, аутосомно-рецессивный и другие, способны передавать разным поколениям мутантные гены.
Особенности наследования аутосомно-доминантного типа
Аутосомно-доминантный тип наследования заболевания характеризуется передачей мутантного гена в гетерозиготном состоянии. У потомства, получившего мутантный аллель, может проявиться генное заболевание. При этом вероятность проявления измененного гена у мужчин и женщин одинаковая.

При проявлении у гетерозигот признак наследования не оказывает серьезного влияния на здоровье и функцию к воспроизводству. Гомозиготы с мутантным генном, который передал тип наследования аутосомно-доминантный, как правило, нежизнеспособны.
У родителей мутантный ген располагается в половой гамете совместно со здоровыми клетками, и вероятность его получения у детей будет равняться 50 %. Если доминантный аллель будет изменен не полностью, то дети таких родителей будут полностью здоровы на генном уровне. При низком уровне пенентрантности мутантный ген может проявляться не в каждом поколении.
Чаще всего тип наследования аутосомно-доминантный передает заболевания из поколения в поколение. При этом виде наследования у больного ребенка один из родителей болеет тем же заболеванием. Однако, если в семье болеет только один родитель, а второй имеет здоровые гены, то дети могут и не получить по наследству мутантный ген.
Пример наследования по аутосомно-доминантному типу
Тип наследования аутосомно-доминантный может передавать более 500 разных патологий, среди них: синдром Марфана, Элерса-Данло, дистрофия, болезнь Реклингхайзена, Гентингтона.
При изучении родословной можно проследить аутосомно-доминантный тип наследования. Примеры этому могут быть разные, но самый яркий – это болезнь Гентингтона. Она характеризуется патологическими изменениями нервных клеток в структурах переднего мозга. Проявляется недуг забывчивостью, слабоумием, проявлением непроизвольных телодвижений. Чаще всего это заболевание проявляется после 50 лет.

При прослеживании родословной можно выяснить, что хотя бы один из родителей страдал такой же патологией и передал ее по аутосомно-доминантному типу. Если же у больного есть брат или сестра единокровные, но у них нет проявления болезни, значит, родители передали патологию по гетерозиготному признаку Аа, при котором генные нарушения встречаются у 50 % детей. Следовательно, у потомства больного также могут родиться 50 % детей с видоизмененным геном Аа.
Аутосомно-рецессивный тип
При аутосомно-рецессивном наследовании отец и мать являются носителями патогена. У таких родителей 50 % детей рождаются носителями, 25 % — здоровыми и столько же — больными. Вероятность передачи патологического признака девочкам и мальчикам одинакова. Однако заболевания аутосомно-рецессивного характера могут передаться не каждому поколению, а проявляться через одно-два поколения потомства.
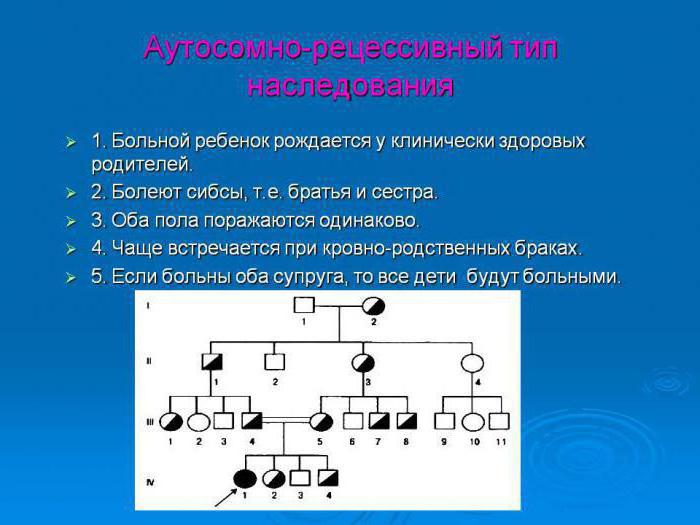
Примером заболеваний, передающихся по аутосомно-рецессивному типу, могут быть:
- болезнь Тоя-Сакса;
- нарушения обмена веществ;
- муковисцидоз и пр.
При обнаружении детей с аутосомно-рецессивным типом генных патологий выясняется, что родители находятся в родственной связи. Такое часто наблюдается в закрытых поселениях, а также в местах, где разрешаются кровные браки.
Х-хромосомное наследование
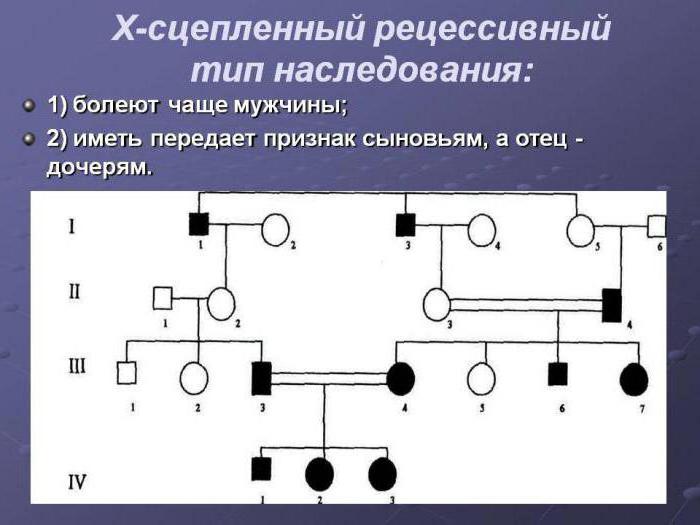
Х-ромосомный тип наследования у девочек и мальчиков проявляется по-разному. Это обусловлено наличием сразу двух Х-хромосом у женщины и одной у мужчины. Женский пол получает свои хромосомы по одной от каждого родителя, а мальчики – только от матери.
По этому типу наследования чаще всего патогенный материал передается женщинам, так как у них больше вероятности получить патогены от отца или матери. Если же носителем доминантного гена в семье является отец, то все мальчики будут здоровы, а у девочек будет проявляться патология.
При рецессивном типе Х-сцепления хромосом болезни проявляются у мальчиков с гемизиготным типом. Женщины всегда будут носителями больного гена, так как они гетерозиготные (в большинстве случаев), но если у женского пола будет гомозиготный признак, то она может заболеть.
Примером патологий с рецессивной Х-хромосомой могут быть: дальтонизм, дистрофия, болезнь Хантера, гемофилия.
Митохондриальный тип
Данный тип наследования является относительно новым. Митохондрии передаются с цитоплазмой яйцеклетки, в которых более 20 000 митохондрий. Каждая из них содержит хромосому. При данном типе наследования патологии передаются только по материнской линии. От таких матерей все дети рождаются больными.
При проявлении митохондриального признака наследственности у мужчин рождаются здоровые дети, так как этот ген не может передаваться от отца к ребенку, поскольку в спермии нет митохондрий.
Источник
При аутосомно-доминантном типе наследования абсолютное большинство больных в популяции рождаются в браках между пораженным (гетерозиготным по аутосомно-доминантному гену Аа) и здоровым супругом (гомозиготному по нормальному аллелюаа), когда возможны следующие варианты генотипов у потомства (рис.).
Таким образом, вероятность получения поражённого гена А составляет 50%; отношение числа здоровых детей в потомстве к числу пораженных равно 1:1 и не зависит от пола ребенка.
Среди моногенных заболеваний с аутосомно-доминантным типом наследования наиболее часто встречаются: семейная гиперхолестеринемия, гемохроматоз, синдром Марфана, нейрофиброматоз 1-го типа (болезнь Реклингхаузена), синдром Элерса—Данло, миотоническая дистрофия, ахондроплазия, несовершенный остеогенез и другие. Типичным примером аутосомно-доминантного заболевания является синдром Марфана(рис.) – наследственное заболевание, представляющее собой генерализованное поражение соединительной ткани с высокой пенетрантность и различной экспрессивностью. Частота – 1:10 000. В основе болезни лежит мутация в гене фибриллина — белка, входящего в состав соединительной ткани и обеспечивающего ее упругость. Ген локализован на 15-й хромосоме в участках 15q21.1. В клинической картине синдрома – поражение трех систем организма: опорно-двигательной, сердечно-сосудистой и органов зрения. Для больных характерны высокий рост, астеническое телосложение., непропорционально длинные пальцы (арахнодактилия, или «паучьи» пальцы), долихоцефальный череп, деформация грудной клетки (воронкообразная или килевидная), искривление позвоночника (сколиоз, кифоз), гиперподвижность суставов, плоскостопие. Со стороны сердечно-сосудистой системы наиболее характерны пролапс митрального клапана, расширение аорты в восходящем или брюшном отделе с развитием аневризмы. Патология органов зрения в виде миопии высокой степени связана с подвывихом (или смещением) хрусталика, гетерохрония (разный цвет) радужки. Нередко отмечаются паховые, бедренные, диафрагмальные грыжи. В редких случаях описаны опущение почек, эмфизема легких, тугоухость и глухота. Психическое и умственное развитие больных соответствует норме. Прогноз для жизни и продолжительность жизни определяются степенью поражения сердечно-сосудистой системы.
Рис. Родословная с аутосомно-доминантным типом наследования заболевания (синдром Марфана)
Рис. Родословная с аутосомно-доминантным типом
наследовани с неполной пенетрантностью
(синдром Ваарденбурга)
В ряде случаев, при аутосомно-доминантных заболеваниях, наблюдаются «проскакивания» поколения (рис. ).
Для доминантно наследуемых заболеваний характерен широкий клинический полиморфизм.Больные с аутосомно-доминантными формами патологии часто социально адаптированы, могут иметь детей. Однако при отдельных аутосомно-доминантных заболеванияхотмечаетсяснижение или полное нарушение репродуктивной функции.
Таким образом, основными признаками аутосомно-доминантного типа наследования заболевания, являются:
1) заболевание проявляется в каждом поколении без пропусков (исключения составляют случаи новой мутации или неполной пенетрантности (проявляемости) гена);
2) каждый ребенок родителя, больного аутосомно-доминантным заболеванием, имеет 50%-ный риск унаследовать это заболевание;
3) лица мужского и женского пола поражаются одинаково часто и в одинаковой мере;
4) наблюдается «вертикальный» характер передачи заболевания в родословной, т.е. больной ребенок имеет больного родителя;
5) непораженные члены семьи свободны от мутантного гена, и в этой связи риск рождения больного ребенка сопоставим с частотой мутации.
Источник
ГЕННЫЕ БОЛЕЗНИ
Генные болезни – это разнообразная по клинической картине группе заболеваний, обусловленная мутациями единичных генов.
При генных болезнях наблюдаются два вида изменения белковых продуктов:
· болезни, связанные с качественными изменениями белковых молекул
· заболевания характеризующиеся количественными изменениями содержания нормального белка в клетке (повышенное, пониженное), что вызвано чаще всего мутациями функциональных генов.
Как и для любой группы заболеваний, классификация генных болезней условна и многокомпонентна. По меньшей мере, три разных принципа могут быть положены в основу классификации генных болезней: генетический, клинический, патогенетический. В соответствии с генетическим принципом классификации генные болезни можно подразделить на группы согласно типам наследования:
· аутосомно-доминантные,
· аутосомно-рецессивные,
· сцепленные с половыми хромосомами
Отнесение болезни к той или иной группе помогает врачу сориентироваться относительно ситуации в семье и определить вид медико-генетической помощи.
Аутосомно-рецессивные заболевания.
Известно более 1600 таких болезней. Аутосомно-рецессивные заболевания проявляются только у гомозигот, которые получили по одному рецессивному гену от каждого из родителей. Аутосомно-рецессивные болезни чаще всего обусловлены дефектами ферментов, реже — дефектами структурных белков. Именно поэтому многие врожденные нарушения обмена веществ попадают в эту группу болезней.
Нарушения аминокислотного обмена.
Самая многочисленная группа наследственных болезней обмена веществ. Почти все они наследуются по аутосомно-рецессивному типу.
Фенилкетонурия
— аутосомно-рецессивная болезнь аминокислотного обмена.
Частота в европейских странах 1:10000 новорожденных.
Эта болезнь характеризуется дефицитом печеночного фермента фенилаланингидроксилазы. Локус фенилкетонурии (фенилаланингидроксилазы) расположен в длинном плече 12-й хромосомы.
Ребенок рождается бессимптомном заболевания, но с началом кормления в организм начинает поступать фенилаланин с молоком матери и возникают первые симптомы. В первые месяцы жизни ребенок может быть беспокойным или вялым, снливым. Отмечается гипопигментация кожи, волос, радужной оболочки. От ребенка исходит «мышиный запах». У части детей наблюдается микроцефалия. К полугодию выявляется задержка психомоторного развития. В это же время изменения на коже и судорожные приступы.
Ранняя диагностика фенилкетонурии и профилактическое лечение (искусственная диета) предупреждают развитие клинической картины болезни.
Дети, родившиеся с таким диагнозом, еще некоторое время назад были обречены на тяжелую умственную отсталость, поскольку поступающий с пищей фенилаланин не подвергался необходимым превращениям. В результате страдали функции мозга. Сейчас можно избежать столь тяжелых последствий, если сразу же после рождения больного ребенка исключить из пищи продукты, содержащие фенилаланин. Такие диеты разработаны и применяются. Диагностика фенилкетонурии у новорожденных не представляет трудностей, поэтому при всеобщем скрининге новорожденных и применении диетотерапии частота умственной отсталости вследствие фенилкетонурии может быть снижена. Диагноз ставится на основании клинической картины и результатов биохимического исследования мочи (фенилпировиноградная кислота) или крови (фенилаланинемия).
Нарушение липидного обмена.
Наследственные болезни обмена липидов — обширная группа различных по генезу состояний, патогенетически связанных с нарушением жирового обмена, в том числе — плазматические липидозы, для которых характерно накопление липидных субстанций внутри клеток.нарушения обмена липопротеидов.
Болезнь Тея-Сакса— это аутосомно-рецессивное генетическое заболевание, которое вызывает прогрессирующее ухудшение умственных и физических способностей ребенка. В основе заболевания лежит нарушение обмена ганглиозидов, сопровождающееся повышением их уровня в сером веществе мозга в 100-300 раз. Ганглиозиды накапливаются также в печени, селезенке. При болезни Тея-Сакса определяется дефицит гексозамининидазы А — одной из форм лизосомального фермента. Локализация гена — на 15-й хромосоме. Частота заболевания 1 : 250 000, среди евреев-ашкенази — 1 : 4000.
При рождении и в первые 3-4 мес жизни дети не отличаются от здоровых сверстников. Заболевание развивается медленно, ребенок становится менее активным, теряет приобретенные навыки, утрачивает интерес к игрушкам. Психомоторные нарушения начинают развиваться у детей с 4-6 мес. Дети становятся апатичными, перестают интересоваться окружающим, у них наблюдается мышечная гипотония. К концу 1 -го года жизни развивается слепота, обусловленная атрофией зрительных нервов; интеллект снижается до уровня идиотии. Постепенно развивается полная обездвиженность, наблюдаются судороги, не поддающиеся терапии. Смерть обычно наступает в возрасте 2-4 года.
Болезнь Гоше
Болезнь Гоше (керазиновый ретикулоэндотелиоз, цереброзидоклеточный липидоз) — редкое семейное заболевание, обусловленное накоплением в ретикулогистиоцитарных клетках глюкоцереброзида. В большинстве случаев болезнь наследуется по аутосомно-рецессивному, некоторых случаях — по доминантному типу. В общей популяции данная патология встречается у из 60 000 человек. Основные нарушения имеются на первом этапе утилизации глюкоцереброзида и обусловлены дефицитом глюкоцереброзидазы. Активность фермента при хронической форме болезни Гоше снижена на 65 %, а при острой — практически отсутствует.
Основные проявления болезни Гоше обусловлены накоплением клеток, перегруженных «шлаками», и нарушением функции этих клеток. Накопление клеток в различных органах приводит к увеличению их размеров (селезенка, печень) и нарушению структуры и функции (кости, костный мозг, легкие). Нарушение работы клеток (макрофагов), перегруженных шлаками, имеет следствием развитие малокровия, кровоточивости, истощения, хрупкости костей, болевых кризов. Это связано с тем, что круг «профессиональных обязанностей» макрофагов в организме человека очень широкий и включает регуляцию многих жизненно важных процессов: кроветворения, свертывания крови, обмена костной ткани и др.
Наиболее типичными проявлениями болезни Гоше служат увеличение размеров селезенки и печени, развитие анемии, тромбоцитопении, хронические боли в костях или развитие внезапных приступов сильнейших болей в костях (костные кризы). Последние сопровождаюются лихорадкой и местными островоспалительными явлениями (отек, покраснение), напоминающими картину остеомиелита. Реже болезнь может впервые проявиться переломом кости вследствие незначительной травмы. Поражение костей зачастую представляет основную клиническую проблему и может привести к тяжелой инвалидизации (обездвиженность вследствие многочисленных патологических переломов, деформации костей и суставов, необходимость замены разрушенных тазобедренных или плечевых суставов).
Выделяются три типа болезни Гоше:
— тип I – характеризуется отсутствием признаков поражения нервной системы;
— тип I I (острый нейронопатический) – встречается у детей раннего возраста и отличается тяжелым поражением головного мозга, больные редко доживают до возраста 2 лет;
— тип I I I (хронический нейронопатический) – объединяет более разнородную группу больных, у которых признаки поражения нервной системы могут проявляться как в раннем, так и в подростковом возрасте.
Тип I является наиболее частым клиническим вариантом болезни Гоше и встречается как у детей, так и взрослых. Средний возраст больных в момент диагностики заболевания варьирует от 30 до 40 лет. Спектр клинических проявлений — очень широкий: на одном конце — «бессимптомные» пациенты (заболевание может случайно обнаруживаться при диспансерном обследовании), на другом — больные с тяжелым течением: массивным увеличением печени и селезенки, глубокой анемией и тромбоцитопенией, выраженным истощением и развитием тяжелых, жизненно опасных осложнений (кровотечения, инфаркты селезенки, разрушение костей). В промежутке между этими полярными клиническими группами находятся больные с умеренным увеличением селезенки и почти нормальным составом крови, с наличием или без поражения костей.
Тяжесть клинических признаков при болезни Гоше находится в прямой зависимости от энзимного дефекта. Чем больше снижена активность фермента, тем в более раннем возрасте и в более тяжелой форме проявляется заболевание.
Сфингомиелиноз (болезнь Нимана-Пика)
— внутриклеточный липидоз, характеризующийся накоплением в клетках ретикулоэндотелия фосфолипида сфингомиелина из-за нарушения активности сфингомиелиназы. Тип наследования — аутосомно-рецессивный. Частота заболевания составляет 1:10 000. Болезнь генетически гетерогенна: выделяются 4 варианта — А, В, С, D. При вариантах А и В отмечается дефицит сфингомиелиназы, при вариантах С и D активность энзима нормальная.
Заболевание встречается только в раннем детском возрасте и характеризуется злокачественным течением. Начало заболевания сопровождается отказом от еды, срыгиванием и рвотой. Затем выявляются задержка психомоторного развития и прогрессирующая гепатоспленомегалия. В дальнейшем развиваются спастический тетрапарез, глухота и слепота. Наблюдается умеренное генерализованное увеличение лимфатических узлов. Кожа приобретает коричневый оттенок. На глазном дне обнаруживается вишнево-красное пятно. При варианте болезни А (классическая форма) имеются тяжелые поражения нервной системы, которые сочетаются с выраженной гепатоспленомегалией. Вариант В отличается более поздними сроками манифестации (2- 6 лет), отсутствием неврологической симптоматики и хроническим течением. Чрезвычайной вариабельностью начала характеризуется вариант болезни С, при котором у 40% больных отмечается пролонгированная желтуха, исчезающая к 2-4 мес жизни, типична гепатоспленомегалия. Вариант D по клинической картине сходен с вариантом С, у больных часто наблюдаются миоклонические судороги.
Нарушение обмена гормонов.
Адреногенитальный синдром относится к группе наследственных нарушений биосинтеза стероидных гормонов. Известно несколько разновидностей наследственных дефицитов ферментов, обеспечивающих синтез стероидов. Ген стероид-21-гидроксилазы (СУР21В) локализован в коротком плече 6-й хромосомы. Частота дефицита 21-гидроксилазы — 1:5000 новорожденных. Недостаточность 21-гидроксилазы определяет до 90% всех случаев врожденной гиперплазии надпочечников. Известны два классических варианта этой болезни — сольтеряющая и простая вирильная форма. Другие формы встречаются значительно реже.
Сольтеряющая форма характеризуется полным дефицитом фермента и проявляется нарушением солевого обмена (дефицит минералокортикоидов). В патологический процесс вовлекается ренин-ангиотензинная система. У новорожденного отмечаются срыгивание, рвота, симптомы недостаточности периферического кровообращения, сонливость, потеря массы тела. Обезвоживание вызывает повышенную жажду. При биохимических исследованиях выявляются гиперкапиемия, гипонатриемия, ацидоз.
Простая вирильная форма характеризуется прогрессирующей вирилизацией, ускоренным соматическим развитием, повышенной экскрецией гормонов коры надпочечников. У новорожденных девочек при кариотипе 46,XX отмечается различная степень маскулинизации (от умеренной гипертрофии клитора до полного срастания губно-мошоночных складок с формированием мошонки и пениса). У мальчиков заболевание проявляется на 5-7-м году жизни преждевременным половым развитием.
ГЕННЫЕ БОЛЕЗНИ
Генные болезни – это разнообразная по клинической картине группе заболеваний, обусловленная мутациями единичных генов.
При генных болезнях наблюдаются два вида изменения белковых продуктов:
· болезни, связанные с качественными изменениями белковых молекул
· заболевания характеризующиеся количественными изменениями содержания нормального белка в клетке (повышенное, пониженное), что вызвано чаще всего мутациями функциональных генов.
Как и для любой группы заболеваний, классификация генных болезней условна и многокомпонентна. По меньшей мере, три разных принципа могут быть положены в основу классификации генных болезней: генетический, клинический, патогенетический. В соответствии с генетическим принципом классификации генные болезни можно подразделить на группы согласно типам наследования:
· аутосомно-доминантные,
· аутосомно-рецессивные,
· сцепленные с половыми хромосомами
Отнесение болезни к той или иной группе помогает врачу сориентироваться относительно ситуации в семье и определить вид медико-генетической помощи.
Аутосомно-доминантные заболевания
Известно более 3700 таких болезней. Как правило, они обусловлены дефектами структурных белков или нарушениями регуляции экспрессии (выраженности)генов.
Эти болезни поражают мужчин и женщин с одинаковой частотой. Исключение составляют аутосомные дефекты, наследование которых зависит от пола. Для аутосомно-доминантных болезней характерен фенотипический полиморфизм ( внутри одной семьи).
Синдром Марфана (СМ)
Синдром Марфана — наследственная доминантная болезнь соединительной ткани.
Причиной синдрома Марфана являются мутации в гене фибриллина (локализация в хромосоме 15q).
Наиболее специфичными для синдрома Марфана являются нарушения скелета, вывих хрусталика, сердечно-сосудистые изменения, эктазия твердой мозговой оболочки.
1. Мышечно-скелетная система: арахнодактилия, высокий рост, длинные конечности, деформация позвоночника (сколиоз, грудной лордоз, гиперкифоз), деформация передней стенки грудной клетки (вдавленная грудь, «куриная» грудь или оба варианта), ненормальная подвижность суставов (гиперподвижность, врожденные контрактуры или оба варианта), плоская стопа, высокое арковидное нёбо, недоразвитие вертлужной впадины, мышечная гипотония.
2. Глаза: вывих хрусталика, миопия, отслоение сетчатки, большая роговица, удлиненная ось глазного яблока, уплощение роговицы.
3. Сердечно-сосудистая система: аортальная регургитация, аневризма восходящей части аорты, расслоение аорты, митральная регургитация, застойные сердечные нарушения, пролапс митрального клапана, кальцификация митрального отверстия, аритмия.
4. Наружные покровы: паховые грыжи, атрофические стрии.
5. Легочная система: спонтанный пневмоторакс.
6. Нервная система: эктазия твердой мозговой оболочки, аномалии развития нервной системы.
При синдроме Марфана ростовые скачки и закрытие зон роста скелета наблюдаются на 2,4 года раньше у лиц мужского пола и на 2,2 года раньше у лиц женского пола. Рост взрослых мужчин равен в среднем 191 см, женщин — 175 см.
Частота синдрома Марфана в популяции равна 1:10 000- 1:15 000. Популяционных и этнических различий в частоте и клинической картине болезни не отмечено.
Нейрофиброматоз (болезнь Реклингхаузена).
Тяжелая многосистемная болезнь с аутосомно-доминантным типом наследования. Распространенность нейрофиброматоза I типа равна примерно 1:3500-5000 новорожденных, одинакова у обоих полов, у всех рас и этнических групп. Ген расположен на 17 хромосоме.
Симптоматика НФ разнообразна, в патологический процесс вовлекаются несколько систем. Диагноз НФ можно поставить при наличии у пациента не менее двух из перечисленных признаков, но при условии, что они не являются симптомами какой-нибудь другой болезни:
1) светло-коричневые пятна на коже; пигментные пятна появляются в детстве, и их число увеличивается с возрастом;
2) наличие двух и более нейрофибром любого типа или одной плексиформной нейрофибромы; их количество с возрастом увеличивается;
3) множественные, похожие на веснушки пигментные пятна в подмышечной ямке, паховой области, на других участках тела со складками;
4) костные изменения (дисплазия крыла крыловидной кости, врожденное искривление или утончение длинных трубчатых костей, ложный сустав);
5) глиома зрительного нерва; узелки Лиша (два и более) на радужной оболочке.
Лечение нейрофиброматоза I типа в основном хирургическое или симптоматическое. В настоящее время идет разработка патогенетической терапии (антифиброзные средства).
Серповидноклеточная анемия.
Характеризуется присутствием неправильных красных кровяных клеток (эритроцитов), устойчивой, серповидной формы. Ее наледование зависит от доминантного гена S, ответсвенного за синтез гемоглобина HbS. Симптомы:
-всегда наблюдается анемия, которая может привести к потере сознания, делает больного физически менее выносливым и может вызвать желтуху (связанную с чрезмерным распадом гемоглобина).
-первыми признаками серповидноклеточной анемии у младенца обычно являются опухание и болезненность кистей рук или стоп, слабость и искривление конечностей и иногда, несколько позднее, отказ от ходьбы.
-ребенок с серповидноклеточной анемией обычно выглядит бледным, возможно, слегка желтушным, но в остальных отношениях, как правило, здоров.
-у взрослых с серповидноклеточной анемией могут обнаруживаться симптомы хронической (постоянной или длительной) закупорки капилляров легких и почек, и может развиться хроническая легочная или почечная недостаточность. Эти два осложнения приводят к ранней смерти некоторых пациентов с серповидноклеточной анемией.
Патология зрения: катаракта и глаукома. Кактаракта – помутнение хрусталика. Глаукома – следствие повышенного внутриглазного давления. Оба заболевания приводят к слепоте, но в настоящее время излечиваются оперативным путем.
Патология скелета:брахидактилия — аномалия развития рук или ног, укорочение пальцев.
Полидактилиия — анатомическое отклонение, характеризующееся бо́льшим, чем в норме, количеством пальцев на руках или ногах у человека.
Синдактилия — проявляется в полном или неполном сращивании пальцев кисти или стопы в результате не наступившего их разъединения в процессе эмбрионального развития.
Ахондроплазия – общее заболевание костной системы: нарушение роста эпифизарных хрящей трубчатых костей, деформация основания черепа и носовых костей. Это приводит к развитию очень коротких конечностей при нормальном туловище и голове.
Источник
