Что такое гемолитическая болезнь у плода
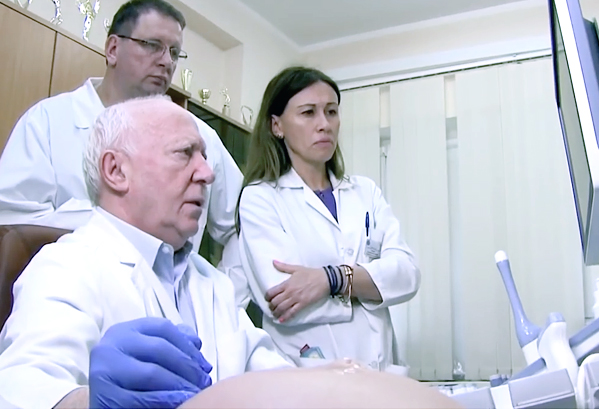
Гемолитическая болезнь плода – внутриутробный иммунологический конфликт, обусловленный несовместимостью крови плода и матери по ряду антигенов, что приводит к гемолизу эритроцитов ребенка под влиянием материнских антител, преодолевающих плацентарный барьер. Гемолитическая болезнь плода может протекать в отечной, желтушной, анемической форме и даже приводить к внутриутробной гибели плода. В диагностике проводится исследование околоплодных вод (амниоцентез), пуповинной крови, билирубина и гемоглобина у новорожденного. Лечение гемолитической болезни плода требует проведения фототерапии, внутривенной инфузии растворов, обменного переливания крови.
Общие сведения
Патогенетическую основу гемолитической болезни составляют процессы, вызванные иммунологической (антиген-антитело) несовместимостью крови плода и матери. В этом случае имеющиеся в крови у плода антигены наследуются от отца, а в крови матери отсутствуют. Чаще всего (1 случай на 250 беременностей) гемолитическая болезнь плода развивается при конфликте по резус-фактору; также может возникнуть при групповой несовместимости крови и другим менее изученным антигенам. Гемолитическая болезнь плода в 3,5% случаев приводит к перинатальной смертности.
При гемолитической болезни плода под влиянием материнских антител, образующихся к антигенам плода и проникающих через плаценту, у ребенка развивается гемолиз эритроцитов и угнетение гемипоэза. Токсическое воздействие продуктов распада эритроцитов на организм плода (новорожденного) приводит к развитию анемии, увеличению билирубина и бластных (незрелых) эритроцитов.
Гемолитическая болезнь плода
Причины гемолитической болезни плода
Иммунологический конфликт, приводящий к гемолитической болезни плода, чаще всего развивается при изосерологической несовместимости крови по системе Резус (Rh), когда у матери имеется Rh-отрицательная кровь, а у плода – Rh-положительная. В таком случае он носит название резус-конфликт. Изоиммунизация при этом может происходить двумя путями: ятрогенным (при сенсибилизации женщины переливаниями Rh(+) крови в прошлом) или при плодово-материнском трансплацентарном переносе эритроцитов плода в материнский кровоток в процессе беременности и родов. В случае Rh-несовместимости гемолитическая болезнь плода редко бывает сопряжена с первой беременностью; чаще развивается от 2-ой или 3-ей беременности с возрастанием рисков с каждой последующей гестацией.
Другой возможной причиной гемолоитической болезни служит несовместимость крови плода и матери по системе АВ0, т. е. при группе крови матери 0 (I), а у плода любой другой. При этом антигены А и В от плода проникают через плаценту в материнский кровоток и вызывают выработку иммунных α- и β- антител с последующим конфликтом «антиген-антитело». Гемолитическая болезнь плода при АВО-несовместимости имеет более легкое течение, чем при Rh-несовместимости. При АВ0-несовместимости гемолитическая болезнь плода может развиться уже в течение 1-ой беременности.
В относительно редких случаях гемолитическая болезнь плода может быть связана с иммунологическими конфликтами по системам Даффи, Келл, MNSs, Кидд, Лютеран и др. или антигенам P, S, N, М.
Проявления гемолитической болезни плода
У беременных специфической картины патологии не наблюдается; иногда нарастание внутриутробных реакций может вызывать у женщины симптомокомлекс, сходный с гестозом. Гемолитическая болезнь плода может проявляться следующими вариантами: внутриутробной гибелью плода в период с 20 по 30 неделю беременности; отечной, желтушной или анемической формах. Общими проявлениями, характерными для всех форм гемолитической болезни плода, служат наличие нормохромной анемии с увеличением в крови эритробластов, гепатомегалии и спленомегалии.
При отечном варианте гемолитической болезни у плода увеличиваются размеры селезенки, печени, сердца, желез, нарастает гипоальбуминемия. Эти изменения сопровождаются выраженным отеком подкожно-жировой клетчатки, асцитом, перикардитом, плевритом, увеличением массы ребенка в 2 раза по сравнению с нормой. При отечном варианте гемолитической болезни плода отмечается резко выраженная анемия (Er -1-1,5 x 1012/л, Нb 35-50 г/л), эритробластемия, увеличение и отечность плаценты. Тяжелые нарушения обмена могут вызывать внутриутробную гибель плода или смерть ребенка вскоре после родов. Отечную форму гемолитической болезни плода отличает крайне тяжелое течение, что в большинстве случаев приводит к летальному исходу.
При желтушном варианте гемолитической болезни плода ребенок чаще рождается от срочных родов, доношенным, чаще с нормальным цветом кожи. В этом случае гемолитическая болезнь плода проявляется спустя несколько часов после рождения – у ребенка стремительно нарастает желтушная окраска кожи; реже желтуха бывает врожденной. У новорожденных с желтушной формой гемолитической болезни увеличены селезенка, печень, лимфоузлы, иногда сердце, отмечается интенсивный прирост непрямого билирубина в крови.
Гипербилирубинемия опасна возможностью повреждения гепатоцитов, кардиомиоцитов, нефронов, нейронов с развитием билирубиновой энцефалопатии. При ядерной желтухе (билирубиновой интоксикации) ребенок вялый, плохо сосет, часто срыгивает, у него развивается гипорефлексия, рвота, судороги. Критический уровень непрямого билирубина, опасный в плане поражения ЦНС, — более 306-340 мкмоль/л у доношенных и 170-204 мкмоль/л у недоношенных. Следствием билирубиновой энцефалопатии может являться гибель ребенка или последующее отставание в психическом развитии.
При анемической форме гемолитической болезни повреждающее воздействие на плод, как правило, невелико. На первый план выходят анемия, бледность кожи, гепатомегалия и спленомегалия. Тяжесть проявлений гемолитической болезни плода определяется титром антител у беременной и степенью зрелости новорожденного: тяжелее заболевание протекает у недоношенных детей.
Диагностика гемолитической болезни плода
В настоящее время акушерство и гинекология придает важное значение своевременному выявлению и правильному ведению беременности, угрожаемой по развитию гемолитической болезни плода. При постановке беременной на учет у нее определяют группу крови и Rh-фактор, выясняют аналогичные данные отца ребенка, интересуются гемотрансфузионным анамнезом, наличием в прошлом мертворожденных детей, самопроизвольных выкидышей или детей с гемолитической болезнью плода. При угрозе развития гемолитической болезнью плода у женщины в динамике контролируют титр специфически антител.
Пренатальная диагностика гемолитической болезни плода включает проведение акушерского УЗИ, допплерографии маточно-плацентарного кровотока и максимального кровотока в средней мозговой артерии с оценкой функционального состояния развивающегося ребенка. Характерными ультразвуковыми критериями гемолитической болезни плода являются плацентомегалия, многоводие, расширение пуповинной вены; сплено- и гепатомегалия, кардиомегалия, наличие перикардиального выпота, гидроторакса.
Учитывая, что гемолитическая болезнь часто сопровождается гипоксией, проводится кардиотокография с оценкой сердечной деятельности плода. В случае получения данных за гемолитическую болезнь плода требуется проведение инвазивных исследований – кордоцентеза и амниоцентеза под контролем УЗИ. При рождении ребенка сразу определяется его резус и групповая принадлежность, исследуется содержание Hb и билирубина в пуповинной крови.
Лечение гемолитической болезни плода
Лечебными задачами при гемолитической болезни плода служат быстрое выведение из крови ребенка токсических факторов гемолиза – непрямого билирубина и антител, а также повышение функций страдающих систем и органов. Выбор способа родоразрешения женщин с изоиммунизацией определяется состоянием плода, сроком беременности, подготовленностью родовых путей. В случае отсутствия данных за тяжелую форму гемолитической болезни плода, на сроке беременности свыше 36 недель, зрелости шейке матки возможны естественные роды. При тяжелом состоянии плода предпочтительнее кесарево сечение за 2-3 недели до ожидаемого срока.
У новорожденных с гемолитической болезнью плода ежедневно контролируется показатели Hb, Ht, билирубина. При необходимости проводится коррекция анемии эритроцитарной массой, инфузионная дезинтоксикационная терапия. Важной составляющей лечения гемолитической болезни плода служит фототерапия, способствующая разрушению непрямого билирубина в коже ребенка. Светолечение проводится в импульсном или непрерывном режиме с помощью ламп дневного или синего света.
При более тяжелых проявлениях гемолитической болезни плода показано проведение капельного внутрижелудочного введения жидкости и заменного переливания крови. При гемолитической болезни плода, обусловленной Rh-конфликтом, при заменном переливании используется одногруппная Rh (-) кровь. В случае несовместимости по ABO переливается эритроцитная масса 0(I) группы в соответствии с Rh-принадлежностью новорожденного и одногруппная плазма. Развитие отека легких и выраженной дыхательной недостаточности требует проведения ИВЛ; наличие асцита диктует необходимость выполнения лапароцентеза под УЗИ-контролем.
Профилактика гемолитической болезни плода
Заключается в предупреждении Rh-иммунизации женщин – внимательном переливании крови с учетом Rh-принадлежности. Женщинам с Rh(-) кровью категорически не рекомендуется прерывание беременности, наступившей впервые. Методом специфической профилактики Rh-конфликта у женщин с Rh(-) кровью служит введение иммуноглобулина антирезус Rho человека после абортов, родов Rh(+) плодом, внематочной беременности, а также после инвазивной пренатальной диагностики — биопсии хориона, амниоцентеза, кордоцентеза.
Источник
Гемолитическая болезнь плода
Гемолитическая болезнь плода и новорождённого (синоним — эритробластоз плода) классифицируется по 3 степеням в зависимости от тяжести гемолитической анемии и способности плода ее компенсировать без развивающихся поражений печени, портальной обструкции и генерализованного отёка.
Выделяют гемолитическую болезнь лёгкой степени (50%), средней степени (25–30%) и тяжелой степени (20–25%).
Гемолитическая болезнь плода в подавляющем большинстве случаев является следствием резус-сенсибилизации беременной.

Как это происходит?
Первичным ответом иммунной системы матери на попадание в кровоток резус-антигенов является выработка IgM-антител, которые не проникают через плацентарный барьер к плоду из-за большой молекулярной массы. Первичный иммунный ответ после попадания D-антигена в кровоток матери проявляется через определенное время, которое составляет от 6 нед до 12 мес. Именно поэтому большинство резус-отрицательных женщин, как правило, благополучно вынашивают свою первую беременность. При повторном попадании резус-антигенов в сенсибилизированный организм матери происходит быстрая и массивная продукция IgG, которые вследствие низкой молекулярной массы способны проникать через плацентарный барьер. В половине случаев для развития первичного иммунного ответа достаточно попадания 50–75 мл эритроцитов, а для вторичного — 0,1 мл.
Проходя через плацентарный барьер, резус-антитела разрушают эритроциты плода, вызывая гемолитическую анемию и образование в большом количестве непрямого билирубина, что вызывает желтуху. В результате возникает компенсаторное экстрамедуллярное кроветворение, очаги которого локализуются преимущественно в печени плода и неизбежно приводят к нарушению её функций. Развиваются портальная гипертензия, гипопротеинемия, водянка плода, т.е. комплекс нарушений, называемый эритробластозом плода. Это состояние требует лечения плода внутриутробно, либо родоразрешения и лечения новорожденного, если срок беременности и возможности неонатальной службы позволяют подобное лечение провести.
Ведение резус-иммунизированных (сенсибилизированных) беременных
При ведении резус-сенсибилизированных беременных крайне важна информация о предыдущих детях или исходах предыдущих беременностей. Особый акцент ставится на тяжести гемолитической болезни у предыдущего ребёнка.
- В связи с возрастающим риском для плода при последующей беременности важно выяснить, на каком гестационном сроке проявились признаки гемолитической болезни у предыдущего ребёнка и тяжесть гемолитической болезни новорождённого.
- Особенности терапии предыдущего ребёнка, в частности, проводилось ли заменное переливание крови (сколько раз) или фототерапия, косвенно указывают на степень гипербилирубинемии и анемии.
При появлении и нарастании титра резус-антител особое значение приобретают неинвазивные методы оценки тяжести состояния плода:
УЗИ и допплерометрия.
Доплерометрия. В настоящее время для оценки тяжести анемии у плода с 20 недель используется допплерометрический метод, который являясь неивазивным, имеет определяющее значение при выборе тактики ведения сенсибилизированной беременной.
При анемии отмечается значительное повышение скорости кровотока в средней мозговой артерии, которое коррелирует с тяжестью анемии у плода.
Ультразвуковая диагностика. Наиболее точно при УЗИ ставится диагноз отечной формы гемолитической болезни плода.
При выраженной водянке плода отмечают:
- гидроперикард (один из ранних признаков);
- асцит и гидроторакс в сочетании с многоводием (очень неблагоприятный прогностический признак);
- кардиомегалию;
- отёк кожи головы (особенно выражен) и кожи конечностей;
- плохую сократимость и утолщение стенок желудочков сердца;
- увеличение эхогенности кишечника из-за отёка его стенок;
- гипертрофию и утолщение из-за отёка плаценты (структура плаценты гомогенная);
- необычную позу плода, известную как «поза Будды», при которой позвоночник и конечности плода отведены от раздутого живота;
- общее снижение двигательной активности, которое характерно для плода, страдающего тяжёлой гемолитической болезнью.
Тактика ведения беременности при гемолитической болезни плода
В гестационный срок менее 33 недель при наличии у пациентки допплерометрических признаков тяжелой анемии плода, либо проявлений отечной формы гемолитической болезни плода, должно быть предпринято родоразрешение либо внутриутробное переливание крови плоду (в зависимости от возможностей клиники).
В сроках более 33 недель при аналогичных показателях, как правило, принимается решение о досрочном оперативном родоразрешении и переливании крови новорожденному.
Окончательное решение должно быть принято на основании оценки зрелости лёгких плода, данных акушерского анамнеза и показателей гематокрита, гемоглобина, билирубина в крови плода и возможностей перинатальной службы.
Внутриутробное переливание крови плоду проводится в Центре в течение 8 лет.
Внутрисосудистое внутриуробное переливание крови плоду
Является методом выбора в связи с меньшим риском осложнений и возможностью контроля над тяжестью анемии и эффективностью лечения. Кроме того, при данной методике интервал между трансфузиями составляет 1,5-2 недели и роды могут быть отсрочены до достижения плодом более зрелого гестационного возраста.
Бригада специалистов состоит: из врача функциональной диагностики, врача акушера-гинеколога, анестезиолога, гемотрансфузиолога.
Техника. Под контролем УЗИ определяют положение плода и место пункции вены пуповины. Иглой 20-го или 22-го калибра трансабдоминально под контролем УЗИ пунктируют пупочную вену недалеко от места отхождения её от плаценты. Перед внутрисосудистой гемотрансфузией проводится кордоцентез и осуществляется забор крови плода для определения предтрансфузионного гематокрита плода.
Объем донорской крови, необходимый для переливания, рассчитывается индивидуально с учетом предполагаемой массы плода, гематокрита крови плода, гематокрита крови донора и фетоплацентарного объема крови, который соответствует сроку беременности.
Гемотрансфузию проводят с начальной скоростью 1–2 мл/мин. До и после гемотрансфузии эритроцитной массы, обедненной лейкоцитами и тромбоцитами определяют гематокрит плода. Конечный гематокрит определяет адекватность гемотрансфузии.
Желательный конечный гематокрит (после трансфузии) — 45%. При тяжёлой анемии плода с гематокритом ниже 30% трансфузии позволяют поддерживать гематокрит на уровне, близком к нормальному для данного гестационного возраста (45–50%).
Требования к эритроцитной массе: группа крови 0, резус-отрицательная, тестированная и негативная на вирус гепатита В, С, цитомегаловирус и ВИЧ, совместимая с матерью и плодом, отмытая в физиологическом растворе для сведения к минимуму риска вирусного заражения. Интервал между трансфузиями зависит от посттрансфузионного гематокрита и составляет в среднем около 1,5- 2 недель.
Внутрисосудистое внутриутробное переливание крови плоду обеспечивает:
- подавление продукции фетальных эритроцитов (в ответ на меньшее количество резус-положительных клеток снижается стимуляция материнской иммунной системы);
- пролонгирование беременности до более зрелого гестационного возраста плода и предотвращение осложнений, связанных с глубокой недоношенностью.
Роды должны быть предприняты только тогда, когда риск, связанный с преждевременными родами, меньше риска, связанного с внутриуробным переливанием крови плоду, обязательно после проведения профилактики респираторного дистресс-синдрома плода. В типичных случаях это происходит к 33 неделе гестации. Кесарево сечение является оптимальным методом родоразрешения при водянке и тяжёлой анемии у плода, когда имеется высокий риск нарушения его состояния в родах. Во время родов должна присутствовать неонатальная бригада, имеющая в своем распоряжении кровь для заменного переливания.
В целом, мы располагаем опытом многократных внутриутробных переливаний крови плоду с последующим успешным родоразрешением и выхаживанием новорожденных.
Источник
Гемолитическая болезнь новорожденных (ГБН) – патологическое состояние ребенка (плода), которое сопровождается распадом (гемолизом) эритроцитов, обусловленным несовместимостью его крови с материнской по эритроцитарным антигенам.
Общая информация
Эритроциты – клетки красного цвета, которые являются форменными элементами крови человека. Они выполняют очень важную функцию: доставляют кислород из легких к тканям и осуществляют обратный транспорт углекислого газа.
На поверхности эритроцитов находятся агглютиногены (белки-антигены) двух типов А и В, а плазме крови присутствуют антитела к ним – агглютинины α и ß – анти-А и анти-В соответственно. Различные комбинации этих элементов служат основой для выделения четырех групп по системе АВ0:
- 0(I) – нет обоих белков, есть антитела к ним;
- A (II) – есть белок А и антитела к В;
- B (III) – есть белок В и антитела к А;
- AB (IV) – есть оба белка и нет антител.
На оболочке эритроцитов находятся и другие антигены. Наиболее значимый из них – антиген D. При его наличии считается, что кровь обладает положительным резус-фактором (Rh+), а при отсутствии – отрицательным (Rh-).
Группа крови по системе АВ0 и резус-фактору имеет огромное значение во время беременности: конфликт крови матери и ребенка приводит к агглютинации (склеиванию) и последующему разрушению красных клеток, то есть к гемолитической болезни новорожденных. Она обнаруживается у 0,6% детей и без адекватной терапии приводит к тяжелым последствиям.
Причины
Причина гемолитической болезни новорожденных – конфликт крови ребенка и матери. Он возникает при следующих условиях:
- у женщины с резус-отрицательной (Rh-) кровью развивается резус-положительный (Rh+) плод;
- у будущей матери кровь относится к 0(I) группе, а у ребенка – к А(II) либо В(III);
- имеет место конфликт по другим антигенам.
В большинстве случаев ГБН развивается из-за резус-конфликта. Существует мнение, что несовместимость по системе АВ0 встречается еще чаще, но из-за легкого течения патологии ее не всегда диагностируют.
Резус-конфликт провоцирует гемолитическую болезнь плода (новорожденного) только при условии предшествующей сенсибилизации (повышения чувствительности) организма материи. Сенсибилизирующие факторы:
- переливание Rh+ крови женщине с Rh- независимо от возраста, в котором оно было осуществлено;
- предыдущие беременности, в том числе и прерванные после 5-6 недели, – риск развития ГБН увеличивается с каждыми последующими родами, особенно если они были осложнены отслойкой плаценты и хирургическими вмешательствами.
При гемолитической болезни новорожденных с несовместимостью по группе крови, сенсибилизация организма происходит в повседневной жизни – при употреблении некоторых продуктах, во время вакцинации, в результате инфекций.
Еще один фактор, повышающий риск патологии, – нарушение барьерных функций плаценты, происходящее в результате наличия хронических заболеваний у беременной женщины, неправильного питания, вредных привычек и так далее.
Патогенез
Патогенез гемолитической болезни новорожденных связан с тем, что иммунная система женщины воспринимает элементы крови (эритроциты) плода в качестве чужеродных агентов и вырабатывает антитела для их уничтожения.
При резус-конфликте Rh-положительные эритроциты плода проникают в кровь матери с Rh-. В ответ ее организм вырабатывает антирезус-антитела. Они проходят сквозь плаценту, попадают в кровь ребенка, связываются с рецепторами на поверхности его эритроцитов и уничтожают их. При этом в крови плода существенно снижается количество гемоглобина и повышается уровень неконъюгированного (непрямого) билирубина. Так развиваются анемия и гипербилирубинемия (гемолитическая желтуха новорожденных).
Непрямой билирубин – желчный пигмент, обладающий токсичным действием на все органы, – почки, печень, легкие, сердце и так далее. При высокой концентрации он способен проникать через барьер между кровеносной и нервной системами и повреждать клетки мозга, вызывая билирубиновую энцефалопатию (ядерную желтуху). Риск поражения мозга при гемолитической болезни новорожденных увеличивается в случае:
- снижения уровня альбумина – белка, который обладает способностью связывать и обезвреживать билирубин в крови;
- гипогликемии – дефицита глюкозы;
- гипоксии – нехватки кислорода;
- ацидоза – увеличения кислотности крови.
Непрямой билирубин повреждает клетки печени. В результате в крови возрастает концентрация конъюгированного (прямого, обезвреженного) билирубина. Недостаточное развитие у ребенка желчных протоков приводит к его плохому выведению, холестазу (застою желчи) и гепатиту.
Из-за выраженной анемии при гемолитической болезни новорожденных могут возникнуть очаги экстрамедуллярного (внекостномозгового) кроветворения в селезенке и печени. В итоге эти органы увеличиваются, а в крови появляются эритробласты – незрелые эритроциты.
Продукты гемолиза красных кровяных телец накапливаются в тканях органов, обменные процессы нарушаются, и возникает дефицит многих минеральных веществ – меди, кобальта, цинка, железа и других.
Патогенез ГБН при несовместимости по группе крови характеризуется сходным механизмом. Отличие состоит в том, что белки А и В созревают позже, чем D. Поэтому конфликт представляет опасность для ребенка ближе к концу беременности. У недоношенных детей распад эритроцитов не возникает.
Симптомы
Гемолитическая болезнь новорожденных протекает в одной из трех форм:
- желтушной – 88% случаев;
- анемической – 10%;
- отечной – 2%.
Признаки желтушной формы:
- желтуха – изменение цвета кожи и слизистых оболочек в результате накопления пигмента билирубина;
- снижение гемоглобина (анемия);
- увеличение селезенки и печени (гепатоспленомегалия);
- вялость, снижение рефлексов и тонуса мышц.
При конфликте по резусу желтуха возникает сразу после рождения, по AB0-системе – на 2-3 сутки. Оттенок кожи постепенно меняется от апельсинового до бледно-лимонного.
Если показатель непрямого билирубина в крови превышает 300 мкмоль/л, на 3-4 сутки может развиться ядерная гемолитическая желтуха у новорожденных, которая сопровождается поражением подкорковых ядер мозга. Ядерная желтуха характеризуется четырьмя этапами:
- Интоксикация. Для нее характерны потеря аппетита, монотонный крик, двигательная слабость, рвота.
- Поражение ядер. Симптомы – напряженность затылочных мышц, резкий крик, набухание родничка, тремор, опистотонус (поза с выгибанием спины), исчезновение некоторых рефлексов, брадикардия.
- Мнимое благополучие (улучшение клинической картины).
- Осложнения гемолитической болезни новорожденных. Появляются в конце 1 – начале 5 месяца жизни. Среди них – параличи, парезы, глухота, ДЦП, задержка развития и так далее.
На 7-8 день гемолитической желтухи у новорожденных могут возникнуть признаки холестаза:
- обесцвечивание кала;
- зеленовато-грязный оттенок кожи;
- потемнение мочи;
- повышение в крови уровня прямого билирубина.
При анемической форме клинические проявления гемолитической болезни новорожденных включают:
- анемию;
- бледность;
- гепатоспленомегалию;
- незначительное повышение или нормальный уровень билирубина.
Анемическая форма характеризуется наиболее легким течением – общее самочувствие ребенка почти не страдает.
Отечный вариант (внутриутробная водянка) – самая тяжелая форма ГБН. Признаки:
- бледность и сильный отек кожи;
- большой живот;
- выраженное увеличение печени и селезенки;
- вялость мышц;
- приглушение тонов сердца;
- расстройства дыхания;
- тяжелая анемия.
Отечная гемолитическая болезнь новорожденных приводит к выкидышам, мертворождению и гибели детей.
Диагностика
Диагностика ГБН возможна в пренатальный период. Она включает:
- Сбор анамнеза – уточнение количества предыдущих родов, выкидышей и переливаний, выяснение информации о состоянии здоровья старших детей,
- Определение резус-фактора и группы крови беременной, а также отца ребенка.
- Обязательное выявление противорезусных антител в крови женщины с Rh- не менее 3 раз за период вынашивания ребенка. Резкие колебания цифр считаются признаком конфликта. При несовместимости АВ0-системе контролируется титр аллогемагглютининов.
- УЗИ-сканирование – показывает утолщение плаценты, многоводие, увеличение печени и селезенки плода.
При высоком риске гемолитической болезни новорожденных на 34 неделе проводится амниоцентез – забор околоплодных вод через прокол в пузыре. При этом определяется плотность билирубина, уровень антител, глюкозы, железа и других веществ.
После рождения диагноз ГБН ставится на основании клинических симптомов и лабораторных исследований. Анализ крови показывает:
- уровень билирубина выше 310-340 мкмоль/л сразу после рождение и его рост на 18 мкмоль/л каждый час;
- концентрацию гемоглобина ниже 150 г/л;
- снижение числа эритроцитов с одновременным повышением эритробластов и ретикулоцитов (незрелых форм кровяных телец).
Также проводится проба Кумбса (показывает количество неполных антител) и отслеживается уровень противорезусных антител и аллогемагглютининов в крови матери и грудном молоке. Все показатели проверяются несколько раз в сутки.
Гемолитическая болезнь новорожденных дифференцируется от анемии, тяжелой асфиксии, внутриутробной инфекции, физиологической желтухи и других патологий.
Лечение
Лечение тяжелой гемолитической болезни новорожденных в пренатальный период осуществляется путем переливания эритроцитарной массы плоду (через вену пуповины) либо с помощью заменного переливания крови (ЗПК).
ЗПК – процедура поочередного выведения крови ребенка небольшими порциями и введения донорской крови. Она позволяет удалить билирубин и материнские антитела, одновременно восполнив потери эритроцитов. Сегодня для ЗПК используется не цельная кровь, а эритроцитарная масса, смешанная с замороженной плазмой.
Показания к ЗПК для доношенных детей с диагнозом «гемолитическая желтуха новорожденных»:
- билирубин в пуповинной крови выше 60 мкмоль/л и увеличение этого показателя на 6-10 мкмоль/л каждый час, уровень пигмента в периферической крови – 340 мкмоль/л;
- гемоглобин ниже 100 г/л.
В некоторых случаях процедуру повторяют через 12 часов.
Другие методы, применяемые для лечения ГБН новорожденных:
- гемосорбция – фильтрация крови через сорбенты, очищающие ее от токсинов;
- плазмаферез – удаление из крови части плазмы вместе с антителами;
- введение глюкокортикоидов.
Лечение ГБН при легком и среднетяжелом течении, а также после ЗПК или очищения крови включает медикаментозные средства и фототерапию.
Лекарства, используемые при гемолитической болезни новорожденных:
- белковые препараты и глюкоза внутривенно;
- индукторы печеночных ферментов;
- витамины, улучшающие работу печени и активизирующие обменные процессы, – Е, С, группы В;
- желчегонные средства в случае сгущения желчи;
- переливание эритроцитарной массы;
- сорбенты и очистительные клизмы.
Фототерапия – процедура облучения тела ребенка флуоресцентной лампой с белым или синим светом, в ходе которой непрямой билирубин находящейся в коже окисляется, а затем выводится из организма.
Отношение к грудному вскармливанию при ГБН у новорожденных неоднозначное. Ранее считалось, что ребенка можно прикладывать к груди только через 1-2 недели после рождения, поскольку к этому моменту в молоке уже нет антител. Сегодня врачи склоняются к тому, чтобы кормление грудью начиналось с первых дней, поскольку антирезусные антитела разрушаются в желудке ребенка.
Прогноз
Последствия гемолитической болезни новорожденных зависят от характера течения. Тяжелая форма может привести к гибели ребенка в последние месяцы беременности или в течение недели после рождения.
Если развивается билирубиновая энцефалопатия возможны такие осложнения, как:
- церебральный паралич;
- глухота, слепота;
- задержка развития.
Перенесенная гемолитическая болезнь новорожденных в старшем возрасте провоцирует склонность к частым заболеваниям, неадекватные реакции на вакцинацию, аллергию. У подростков наблюдаются снижение работоспособности, апатия, тревожность.
Профилактика
Профилактика гемолитической болезни новорожденных направлена на предупреждение сенсибилизации женщины. Основные меры – переливание крови только с учетом резус-фактора, недопущение абортов и так далее.
Поскольку главным сенсибилизирующим фактором при резус-конфликте являются предыдущие роды, в течение суток после появления первого ребенка с Rh+ (либо после аборта) женщине необходимо ввести препарат с иммуноглобулином анти-D. Благодаря этому эритроциты плода быстро выводятся из кровотока матери и не провоцируют образование антител при последующих беременностях. Недостаточная доза средства или его позднее введение существенно снижают эффективность процедуры.
Профилактика ГБН во время беременности при выявлении Rh-сенсибилизации включает:
- неспецифическую гипосенсибилизацию – введение детоксикационных, гормональных, витаминных, антигистаминных и других препаратов;
- гемосорбцию, плазмаферез;
- специфическую гипосенсибилизацию – пересадку лоскута кожи от мужа;
- ЗПК на сроке 25-27 недель с последующим экстренным родоразрешением.
Источник
