Геморрагическая болезнь новорожденных с поздним дебютом

Среди всех патологических состояний у детей особое место занимают геморрагические нарушения, что обусловлено потенциально высоким риском развития серьезных осложнений [1–3]. Причинами этого, как правило, являются поздняя диагностика и неадекватная терапия.
Несвоевременная нозологическая верификация геморрагического синдрома нередко обусловлена недооценкой анамнестических данных, некорректной трактовкой клинических проявлений, а также ошибками интерпретации результатов лабораторного обследования [1–4]. Кроме этого, в ряде случаев причиной поздно установленного диагноза является терминологическая путаница, в результате которой у практикующего врача-педиатра может сложиться ошибочное представление о возрастных ограничениях для определенных видов геморрагических нарушений.
Так, общепризнанный термин «геморрагическая болезнь плода и новорожденного» (код Р53 по МКБ-10) с формальных позиций должен применяться только в тех случаях, когда витамин-К-дефицитная коагулопатия выявляется в перинатальный период. В то же время доказано, что дефицит витамина К в организме ребенка клинически может манифестировать не только в период новорожденности, но и в последующие недели и даже месяцы жизни [5–9]. В этих случаях говорят о «поздней геморрагической болезни новорожденного». Однако корректность данного термина вызывает обоснованные сомнения, поскольку он применяется для обозначения геморрагического синдрома, проявившегося в постнеонатальный период. Ошибочная привязка дефицита витамина К только к периоду новорожденности создает предпосылки для игнорирования этих состояний при поиске причин геморрагических нарушений у детей в возрасте старше 1 мес. Недооценка роли витамин-К-дефицитных состояний в генезе геморрагического синдрома в постнеонатальном периоде может стать причиной поздней диагностики и риска развития серьезных осложнений. В качестве примера поздней верификации витамин-К-зависимой коагулопатии приводим собственное клиническое наблюдение.
Девочка в возрасте 1 мес. 11 дней с диагнозом «Гастродуоденальный рефлюкс? Эзофагит?» направлена участковым врачом-педиатром на госпитализацию в связи с частыми срыгиваниями и появлением прожилок коричневатого цвета в рвотных массах.
Из анамнеза известно: девочка от соматически здоровой женщины 26 лет. От первой беременности, протекавшей с токсикозом в I триместре. Роды 1-е, самостоятельные на 38 нед., физиологические. Масса тела при рождении – 3100 г, рост – 51 см. Оценка по шкале Апгар – 8–9 баллов. К груди приложена сразу после рождения. Грудь взяла активно. С 3-х сут жизни отмечена иктеричность кожных покровов, что было расценено как проявление физиологической желтухи. В родильном доме вакцинирована против туберкулеза и гепатита В. Выписана из родильного дома на 4-е сут в удовлетворительном состоянии.
Девочка с рождения на грудном вскармливании в свободном режиме. Прибавка массы тела за первый месяц жизни составила 1100 г. На фоне грудного вскармливания с первых дней жизни отмечались необильные срыгивания после кормления, расцененные как проявления младенческой регургитации, терапия не проводилась. В течение 3 нед. у ребенка сохранялась желтушность кожных покровов с постепенным угасанием. За 1 нед. до госпитализации срыгивания участились.
При поступлении в отделение состояние ребенка средней тяжести. Умеренно выраженная вялость. Кожные покровы бледные. На левом плече и в области левой груди плотноватые подкожные узелки до 1,0 и 0,5 см в диаметре соответственно (со слов матери – «из-за застежек-клипсов на распашонке»). Слизистые влажные, чистые. Тоны сердца звучные, ритмичные, нежный систолический шум на верхушке. В легких дыхание пуэрильное. Живот мягкий, доступен глубокой пальпации. Печень +1,0 см. Стул самостоятельный, кашицеобразный, с небольшой примесью слизи. Мочеиспускание свободное. Очаговая и менингеальная симптоматика отсутствует. В рефлюктате – скудные прожилки крови.
При поступлении проведены исследования клинического и биохимического анализов крови, общего анализа мочи, УЗИ внутренних органов с дополнительной оценкой функционального состояния гастроэзофагеальной области (водно-сифонная проба). При этом была выявлены легкая нормохромная, нормоцитарная анемия: HGB 106 г/л, RBC 3,4х1012, MCV 81 фл, MCH 26,1 пг, ЦП 0,93, умеренно выраженный тромбоцитоз: 612х109. В биохимическом анализе крови отмечены незначительная гипербилирубинемия (общий билирубин – 30 мкмоль/л, прямой – 7 мкмоль/л) и умеренное повышение ЛДГ (1020 ед./л). Данные УЗИ внутренних органов свидетельствовали об отсутствии гастроэзофагеального рефлюкса, халазии и пилоростеноза.
В течение 1 сут пребывания ребенка в отделении обратили внимание на продолжающееся кровотечение из мест забора крови для исследований. Учитывая сохраняющийся геморрагический синдром (кровотечение из мест инъекций, прожилки крови в рвотных массах) ребенку были проведены (сito!) клинический анализ крови с ретикулоцитами, нейросонография и коагулограмма. Одновременно детально проанализировали анамнез и клинические данные, что позволило дополнительно выявить следующее:
– отсутствие геморрагических заболеваний в семье;
– в период беременности и после родов (данный временной период изучали, учитывая вскармливание ребенка исключительно грудным молоком) мать не получала лекарственные препараты, которые могли бы повлиять на гемостаз;
– менадиона натрия бисульфит ребенку в роддоме не вводился;
– прожилки крови в рефлюктате появились еще за 1 нед. до госпитализации;
– четко ограниченное изменение цвета кожи (по типу «синячков») до 0,5 и 1,0 см в диаметре над «узелками» в области соска грудной железы слева и левого плеча. При пальпации указанного опухолевидного образования в области левой грудной железы обнаружено геморрагическое отделяемое из соска. После оттока геморрагического отделяемого «узелок» перестал пальпироваться, но ограниченная синева кожи в этом месте сохранилась. Все это позволило рассматривать выявленные «узелки» как подкожные гематомы, которые мама трактовала как проявление травматизации кожи застежками-клипсами детской одежды.
С учетом продолжающегося кровотечения и появившихся клинических признаков анемизации сразу после забора крови была начата неотложная посиндромная терапия: в/в введение менадиона натрия бисульфита (1 мг/кг), свежезамороженной плазмы (СЗП) (20 мл/кг), наложена давящая повязка на места инъекций с гемостатической губкой.
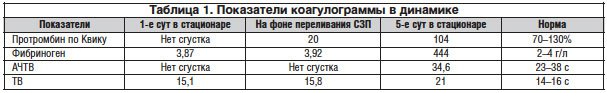
Анализ результатов проведенного (сito!) обследования позволил выявить изменения в клиническом анализе крови в виде появления гипохромной гиперрегенераторной анемии средней тяжести (Нв – 88 г/л, эритроциты – 3,2х1012, цветной показатель – 0,83, ретикулоциты – 5,3%), сохраняющийся тромбоцитоз (621х109) и нормальный уровень длительности кровотечения (по Дуке – 2 мин). При этом по данным коагулограммы обращало на себя внимание отсутствие коагуляции по внутреннему (активированное частичное тромбопластиновое время (АЧТВ) – нет сгустка) и внешнему (протромбиновый индекс – нет сгустка) путям свертывания при нормальных уровне фибриногена (3,81 г/л) и конечном этапе свертывания (тромбиновое время (ТВ) – 15,1 с) (табл. 1). Данные нейросонографии позволили исключить интракраниальные геморрагические изменения.
Полученные результаты лабораторного обследования позволили диагностировать нарушение плазменного гемостаза по типу витамин-К-зависимой коагулопатии. В пользу этого свидетельствовали:
– отсутствие нарушений первичного гемостаза (не было выявлено ни тромбоцитопении, ни пролонгации кровотечения по Дуке);
– наличие нарушений только тех звеньев вторичного гемостаза, функциональная активность которых определяется витамином К. Так, имела место выраженная гипокоагуляция по внутреннему и внешнему путям свертывания, в то время как фибриноген и ТВ оставались в пределах нормы.
Таким образом, данные анамнеза, клиническая картина и результаты обследования позволили верифицировать позднюю геморрагическую болезнь новорожденного, что определило необходимость продолжить терапию менадиона натрием бисульфитом еще в течение последующих 3 дней. При этом следует подчеркнуть, что геморрагический синдром у ребенка был купирован после введения СЗП, в то время как полная нормализация показателей коагулограммы произошла только после окончания курса лечения менадиона натрием бисульфитом (табл. 1).
С учетом того, что дефицит витамина К в организме ребенка мог быть обусловлен не только алиментарным фактором (исключительно вскармливание материнским молоком, характеризующееся низким содержанием витамина К), но и его недостаточным синтезом эндогенной микрофлорой кишечника, а также нарушением его утилизации в кишечнике, были проведены дополнительные обследования. Клинических и лабораторных признаков холестаза и мальабсорбции выявлено не было. Это позволило в качестве основных провоцирующих факторов развития витамин-К-зависимой коагулопатии у данного пациента рассматривать отсутствие профилактического введения менадиона натрия бисульфита в раннем неонатальном периоде и исключительно грудное вскармливание.
Заключительный диагноз: основной – «Поздняя геморрагическая болезнь новорожденного»; осложнения – «Постгеморрагическая анемия средней тяжести»; сопутствующий – «Младенческая регургитация». Амбулаторно рекомендовано продолжение грудного вскармливания при соблюдении мамой рациональной диеты для кормящих женщин и ежедневном приеме поливитаминных препаратов. С целью коррекции анемии назначен полимальтозный комплекс 3-валентного железа (5 мг/кг/сут по элементарному железу) для приема в течение 1 мес. с последующим контролем показателей клинического анализа крови.
Представленный клинический случай свидетельствует о необходимости настороженности врача-педиатра к любым, даже самым минимальным, геморрагическим проявлениям, особенно у детей раннего возраста. При этом замена широко используемого термина «поздняя геморрагическая болезнь новорожденного» на «витамин-К-зависимую коагулопатию» позволит избежать ошибочной привязки витамин-К-дефицитных состояний исключительно к неонатальному периоду. Включение указанного патологического состояния в перечень возможных причин геморрагического синдрома у детей независимо от их возраста позволит своевременно верифицировать диагноз и назначить адекватную терапию.
Литература
1. Баркаган Л.З. Нарушения гемостаза у детей. М., 1993.
2. Nelson Textbook of Pediatrics, 19th Edition /R.M. Kliegman, B.M. Stanton, J. St. Geme, N. Schor, R.E. Behrman. New York, London: Elsevier Inc., 2014.
3. Детские болезни / под ред. Н.П. Шабалова / 6-е изд. СПб.: Питер, 2009.
4. Долгов В.В., Свирин П.В. Лабораторная диагностика нарушений гемостаза. М.: Триада, 2005.
5. Шабалов Н.П. Геморрагические расстройства у новорожденных / В кн.: Неонатология.
В 2-х тт. / 3-е изд., испр. и доп. М.: МЕДпресс-информ, 2004. Т. 2. С. 208–223.
6. Неонатология. Национальное руководство. Крат. изд-е / под ред. Н.Н. Володина. М.: ГЭОТАР-медиа, 2013.
7. Takahashi D., Takahashi Y., Itoh S. et al. Late vitamin K deficiency bleeding in an infant born at a maternity hospital // Pediatr Int. 2014 Jun. Vol. 56 (3). Р. 436.
8. Van Winckel M., De Bruyne R., van de Velde S., van Biervliet S. Vitamin K an update for the paediatrician // Eur J Pediatr. 2009 Feb. Vol. 168 (2). Р. 127–134.
9. Hubbard D., Tobias J.D. Intracerebral hemorrhage due to hemorrhagic disease of the newborn and failure to administer vitamin K at birth // South. Med. J. 2006. Vol. 99 (11). Р. 1216–1220.
Источник
А.И. Лобанов, О.Г. Лобанова
В статье рассмотрены проблемы геморрагической болезни новорожденных с поздним дебютом. В настоящее время в роддомах профилактика геморрагической болезни проводится не всем новорожденным. Проведен клинический анализ 9 случаев болезни. Опасной особенностью позднего проявления геморрагической болезни (после месяца жизни) является развитие массивных внутричерепных кровоизлияний на фоне повышенной кровоточивости. Для позднего возникновения геморрагии вследствие дефицита витамина К характерно сочетание трех факторов: отсутствие профилактики геморрагической болезни, грудное вскармливание ребенка и транзиторный холестаз.
В практике детского реаниматолога нетравматические внутричерепные кровоизлияния у детей первых месяцев жизни встречаются достаточно редко. Установить истинную причину кровоизлияния не всегда возможно. Вместе с тем известно, что одной из причин развития внутричерепных кровоизлияний у детей первых месяцев жизни является поздняя геморрагическая болезнь новорожденных (ГБН). Предвидеть развитие позднего дебюта болезни невозможно, поэтому профилактика ГБН на этапе родильного дома чрезвычайно важна.
Предшествует развитию ГБН у новорожденных, особенно тех, кто находится на естественном вскармливании, дефицит витамина К: в гепатоците нарушается гамма-карбоксилирование витамин К-зависимых факторов свертывания крови. В результате не подвергавшиеся карбоксилированию факторы утрачивают способность участвовать в процессе свертывания крови.
Иммунологически они обнаруживаются в крови в нормальном количестве, в виде некарбоксилированных и нефункционирующих молекул, обозначаемых в литературе аббревиатурой PIVKA {Protein-Induced by Vitamin К Absence) [1].
Эти неполноценные факторы свертывания не способны качественно влиять на процессы коагуляции крови, что приводит к развитию ГБН. Наиболее опасное проявление этой патологии — внутричерепное кровоизлияние, возникающее на фоне общей кровоточивости (кожных геморрагии, желудочно-кишечных кровотечений).
За период с 2004 по 2008 гг. в отделение реанимации ГКБ № 4 г. Ижевска были госпитализированы 9 детей с нетравматическими внутричерепными кровоизлияниями. Возраст пациентов составлял от 1 до 2,5 мес жизни. Шестеро детей госпитализированы из дома и трое — из стационаров города.
Анамнез
При сборе анамнеза было выяснено, что все дети — от практически нормально протекавшей беременности, срочных родов, находившиеся на естественном вскармливании. В роддоме всем новорожденным была проведена вакцинация от гепатита В и БЦЖ. Профилактическое введение менадиона натрия (Викасол) новорожденным не проводилось. На 5-7 сут все дети были выписаны домой. В дальнейшем 2 ребенка были привиты от гепатита В дважды.
Клиника дебюта
Начало заболевания протекало практически одинаково у всех детей. За 1-2 дня до возникновения внутричерепного кровоизлияния на коже или слизистой ротовой полости появлялись геморрагические элементы (табл. 1).

Единичные глубокие экхимозы диаметром от 5 до 20 мм обнаруживались родителями чаще на конечностях, реже — на туловище. Мелкие множественные кровоизлияния на слизистой ротовой полости выявлялись уже при осмотре в реанимации. У одного больного ребенка была обнаружена кровь в стуле и отмечалась длительная кровоточивость из места инъекции при повторной вакцинации от гепатита В. При консультации хирургом патологии не выявлено.
У всех больных внутричерепное кровоизлияние манифестировало внезапным, болезненным, но недлительным плачем. У 8 детей сразу появилась постоянная и упорная рвота, в двух случаях — с примесью крови. Рвота не отмечалась только у одного ребенка. Вначале дети проявляли периодическое беспокойство, начинали стонать, отказывались от кормления, затем становились апатичными и безучастными к окружающему. У 7 детей отмечались тонические судороги. Нарастала резкая бледность кожи. Кратковременная субфебрильная температура сменялась гипотермией.
Практически все дети были очень поздно госпитализированы: время, проведенное дома от момента возникновения кровоизлияния до госпитализации, составляло от одних суток и более. При поступлении в реанимационное отделение 8 детей находились в крайне тяжелом состоянии. У всех определялась декомпенсация легочной вентиляции, расстройства системного кровообращения, очаговая и общемозговая неврологическая симптоматика, нарушения коагуляционного гемостаза. В 6 случаях у поступивших было редкое, аритмичное дыхание или его полное отсутствие. В 2 случаях дыхательные нарушения были только в виде выраженного тахипное (частота дыхания — в пределах 100/мин).
У всех пациентов отмечалась резкая бледность кожи и слизистых с цианотичным оттенком, а также кровоточивость из мест инъекций. У 2 детей наблюдались признаки невыраженного легочного и желудочного кровотечения, в виде геморрагического отделяемого из эндотрахеальной трубки и желудочного зонда. У 8 детей при поступлении сохранялся легкий желтушный оттенок кожи. Дефицит объема циркулирующей крови составлял от 30 до 39% от нормы (норма ОЦК у детей первых месяцев жизни — 85 мл/кг; ОЦКфакт = масса тела/весовая часть ОЦК по гематокриту в таблице). Артериальное давление колебалось от 80/40 до 110/72 мм рт. ст. В 7 случаях у детей отмечалась тахикардия с глухостью сердечных тонов. В неврологическом статусе у 6 детей наблюдались нарушения центральной регуляции дыхания. Патологические формы дыхания в виде выраженного брадипноэ или апноэ у этих детей развились еще до момента госпитализации и продолжали прогрессировать до полной утраты автоматического дыхания. Стволовые рефлексы со слизистых (роговицы, глотки, трахеи) не вызывались. Отмечалась резкая сухость и отек слизистых ротовой полости, склер. Отсутствовал окулоцефалический рефлекс. Выявлялся фиксированный, двусторонний, паралитический мидриаз, диффузная мышечная атония.
У всех детей большой родничок был выбухающим, плотным на ощупь, с отсутствием пульсации. Отмечалась резкая гипотермия кожи головы. У 5 детей отмечались приступы горметонии (периодическое тоническое напряжение мышц конечностей и туловища, возникающее на фоне мышечной атонии спонтанно или под влиянием раздражителей, длящееся не более 10 с). В данном случае появление горметонии связано с повреждением ствола на уровне среднего мозга и моста вследствие транстенториального вклинения, когда происходит функциональное разобщение ствола и полушарий большого мозга. По мере углубления комы приступы горметонии прекращались. Таким образом, у всех 6 больных была констатирована кома 3 степени (запредельная). Все больные, поступившие в отделение реанимации в состоянии запредельной комы, погибли.
У двоих детей при поступлении в реанимацию была констатирована кома 1-2 степени. Отмечались тонические судороги, преходящие симптомы поражения III, VI, VII пары черепно-мозговых нервов, тахипноэ. Большой родничок был плотным, выбухающим, но с сохранением пульсации. Реакция зрачков на свет, стволовые рефлексы со слизистых (роговицы, глотки, трахеи), окулоцефалический рефлекс — оставались сохранными. У одного больного в неврологическом статусе — признаки умеренно выраженной внутричерепной гипертензии.
Лабораторное обследование
В анализах периферической крови у большинства больных отмечалось значительное снижение уровня гемоглобина (табл. 2).
У всех пациентов время свертывания крови (по Моравицу) было резко удлинено. Протромбиновый индекс определялся только у одного больного и был снижен. Количество тромбоцитов было нормальным или повышенным, и имело тенденцию к еще большему повышению в течение суток. Нормальные показатели фибриногена отмечались у 4 больных, у остальных фибриноген не определялся. Прямой билирубин оставался повышенным у 8 детей, печеночные ферменты незначительно повышены — у 1.
Диагностика
У всех детей были выявлены субарахноидальные кровоизлияния. В 8 случаях кровоизлияния были массивными. Диагностика внутричерепных кровоизлияний осуществлялась на основании анамнеза, клинических данных и ультразвуковых исследований. Проведение нейровизуальных методов исследования (КТ, МРТ головного мозга) у подавляющего большинства пациентов было невозможно из-за крайне тяжелого состояния больных. У 3 пациентов после стихания кровоточивости, когда не была запредельно выражена внутричерепная гипертензия (необратимый отек мозга), кровоизлияние подтверждалось люмбальной пункцией (через сутки). Ликвор чаще вытекал под низким или нормальным давлением, красно-бурого цвета. При его центрифугировании выявлялась резкая ксантохромия; при микроскопии обнаруживались в большом количестве измененные (гемолизированные) эритроциты. При биохимическом исследовании ликвора определялись низ¬кий уровень глюкозы и высокие цифры белка, молочной кислоты (лактата).
Терапия
8 детей находились на искусственной вентиляции легких. Всем проводилась коррекция ОЦК, нарушений гемостаза и метаболизма, а также противосудорожная и нейропротекторная терапия. Купирование кровоточивости начиналось с введения через зонд 10 мг Викасола, однократной трансфузии свежезамороженной плазмы в объеме 15 мл/кг. С прекращением кровоточивости (обычно через 10-12 ч) продолжалось дальнейшее введение менадиона натрия (внутримышечно) для создания депо по 5 мг/сут в течение 2-3 дней. 8 пациентам вследствие развития постгеморрагической анемии проводилось переливание эритроцитарной массы. В дальнейшем ни у одного из больных кровоточивости не было.
Результаты аутопсии
На аутопсии у погибших детей были обнаружены массивные субарахноидальные кровоизлияния; в 2 случаях с наличием крови еще и в субдуральном пространстве и в 1 случае — в желудочковой системе мозга. В 2 случаях мозг был в состоянии некроза. Кроме этого, у всех погибших детей обнаружены изменения в печени, чаще всего в виде неспецифического реактивного гепатита с внеклеточным холестазом и начальным фиброзом портальных трактов.
Обсуждение
Входе проведения клинического наблюдения было отмечено, что всех детей, поступивших в отделение реанимации с генерализованной кровоточивостью, объединяет ряд общих факторов и клинических особенностей, характерных для возникновения позднего дебюта ГБН. Основной фактор — отсутствие профилактики ГБН. Частота развития позднего дебюта ГБН без профилактики витамином К, по некоторым данным, составляет 5-20 случаев на 100 тыс. новорожденных [2]. Никому из 9 детей, поступивших в отделение реанимации с генерализованной кровоточивостью, в роддоме не проводили профилактику ГБН введением менадиона натрия.
Второй фактор — грудное вскармливание. Все наблюдаемые дети были доношенными, находились исключительно на грудном вскармливании. В физиологических условиях витамин К (К± или филлохинон) поступает в организм ребенка с пищей (грудное молоко) и дополнительно синтезируется в кишечнике в виде витамина К2 или менахинона. Но синтез витамина К2 в кишечнике происходит преимущественно Bacteroides fragilis и некоторым Escherichia coli — флорой, которая заселяется при искусственном вскармливании.
При естественном вскармливании кишечник заселяется Bifidobacterium, Lactobacillus и Clostridium — флорой, практически неспособной синтезировать витамин К2 [3]. Третий фактор — явления транзиторного холестаза. Они отмечались в 8 случаях. Естественный витамин К всасывается в тонкой кишке при обязательном наличии в ней желчи и жира. Уменьшение тока желчи приводит к мальабсорбции жиров и жирорастворимых витаминов, увеличивая еще больший дефицит витамина К. Новорожденные из-за незрелости экскреторной функции печени особенно предрасположены к холестазу [4].
У 8 из 9 детей, поступивших в реанимацию в возрасте старше 1 месяца жизни, уровень прямого билирубина еще оставался повышенным (от 12 до 27 ммоль/л), что свидетельствует о транзиторной, функциональной и экскреторной недостаточности печени. Из клинических особенностей, характерных для позднего дебюта ГБН, следует отметить: во-первых, развитие массивных внутричерепных кровоизлияний в сочетании с кожными геморрагиями и кровоточивостью из желудочно-кишечного тракта. Во-вторых — отсутствие у наблюдаемых детей в начале заболевания тяжелой патологии с высоким риском развития ДВС-синдрома.
Практически накануне развития поздней ГБН все дети были осмотрены участковыми педиатрами. В-третьих — позднюю госпитализацию этих детей в отделение реанимации. Причиной поздней госпитализации наблюдаемых детей стало то обстоятельство, что повышение внутричерепного давления у детей первых месяцев жизни протекает более медленно в связи с тем, что череп ребенка (до заращения черепных швов и закрытия родничков) остается временно податливым и приспосабливается к возникшим условиям. При попадании крови в подоболочечное пространство мозга угрожаемая симптоматика отсрочена на некоторое время, поэтому родители слишком поздно обратились за медицинской помощью.
В-четвертых — изменения в периферической крови и ликворе. Эти изменения являются приспособительными реакциями саногенетической направленности. Они вызваны кровью, излившейся в подоболочечное пространство, и продуктами ее распада. Поэтому у наблюдаемых детей возникало реактивное повышение температуры тела, отмечались изменения периферической крови в виде лейкоцитоза и сдвига лейкоцитарной формулы влево. Поступление самой крови и продуктов ее распада в ликворное пространство вызывало реактивно выраженный плеоцитоз и гиперпротеинрахию. Эти изменения также носят защитную (саногенетическую) направленность и исчезают по мере очищения ликвора от крови к концу 2-3 нед.
Продукты распада крови обладают выраженной токсичностью (оксигемоглобин, серотонин, билирубин и др.) и дополнительно вызывают резкую церебральную ишемию, приводя к инфаркту мозга. И, наконец, еще одной особенностью поздней ГБН является гипокоагуляционная направленность результатов доступных тестов оценки гемостаза и их стабилизация на фоне введения витамина К (Викасол).
Основой лабораторной диагностики ГБН является определение протромбинового времени и индекса, отражающих суммарно уровень (трех из четырех) зависимых от витамина К факторов свертывания (II, VII, X) (табл. 3).

При ГБН содержание тромбоцитов и тромбиновое время должны быть нормальными [5]. У 8 наблюдаемых детей протромбиновый индекс не определялся, а у 1 был снижен. Ни в одном из наблюдений не выявлено снижения числа тромбоцитов, напротив, в ответ на длительное кровотечение в 7 случаях развился компенсаторный тромбоцитоз. Это обстоятельство исключает вовлеченность тромбоцитов в патологические реакции потребления, связанные с ДВС-синдромом.
При отсутствии клинических признаков ДВС-синдрома у более половины больных при поступлении фибриноген не определялся. Это обусловлено рядом причин, таких как снижение белково-синтетической функции печени при развитии критического состояния, влияние гиповолемии, гипоксии, ацидоза. При классической форме ГБН, возникающей у новорожденных в родильном доме, в отличие от ее поздней формы, не возникает внутричерепных кровоизлияний, такой остроты и декомпенсации витальных функций.
Заключение
На основании проведенного клинического наблюдения можно заключить, что возникновению поздней ГБН подвержены доношенные новорожденные, у которых стало возможным сочетание таких факторов, как отсутствие профилактического введения менадиона натрия, грудное вскармливание и транзиторный холестаз. У новорожденных при предполагаемом грудном вскармливании профилактика ГБН особенно актуальна.
СПИСОК ЛИТЕРАТУРЫ
1. Баркаган 3. С. Введение в клиническую гемостазиологию. — М.: Ньюдиамед-АО, 1998. — С. 21-23.
2. Долгов В. В., Свирин П. В. Лабораторная диагностика нарушений гемостаза. — М.: Триада, 2005. — 213 с.
3. Гусель В. А., Маркова И. В. Справочник педиатра по клинической фармакологии. — Ленинград, 1989. — С. 161-163.
4. Шабалов Н. П. Неонатология. Том 2. — СПб., 1996. — С. 95. 5. Баркаган 3. С. Геморрагические заболевания и синдромы. — М.: Медицина, 1988. — 498 с.
Читать статью на сайте www.evrika.ru
Источник
