Экологически зависимые болезни и их особенности
К экологически зависимым заболеваниям населения относят те болезни, в этиологии которых определенную роль играют факторы окружающей среды. Нередко в этом случае используются термины: «экоболезнь», «антропоэкологические заболевания», «экологически зависимые болезни», «экопатология», «болезни цивилизации», «болезни образа жизни» и т.п. В этих терминах, как видно, акцент делается на экологическую или социальную обусловленность многих заболеваний.
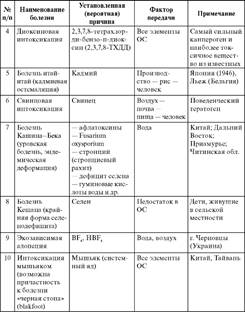
В зависимости от характера (физический, химический, биологический и т.д.) фактор окружающей среды может играть различную роль в этиологии заболевания. Он способен выступать как этиологический, причинный, практически определяющий развитие конкретного специфического заболевания. В настоящее время примерно 20 хронических болезней населения достаточно аргументированно связывают с воздействием экологических факторов (болезнь Минамата, обусловленная загрязнением ртутьсодержащими промышленными стоками морской и речной фауны; болезнь итай-итай, как следствие полива рисовых полей водой, содержащей кадмий, и др.)
Если фактор окружающей среды выступает в качестве причины заболевания, то его эффект носит названиедетерминированного.

Фактор окружающей среды может выступать в роли модифицирующего, т.е. изменять клиническую картину и утяжелять течение хронического заболевания. В этом случае риск, ассоциируемый с определенным фактором, видоизменяется в зависимости от присутствия другого фактора или воздействия. Например, загрязнение атмосферного воздуха оксидами азота провоцирует симптомы нарушения функции дыхательных путей у больных с хроническими респираторными заболеваниями.
В ряде случаев исследуемый фактор может оказывать смешивающее влияние. Примером смешивающих факторов могут служить возраст и табакокурение при изучении влияния атмосферных загрязнений на риск развития заболеваний органов дыхания, табакокурения при изучении риска развития рака легких и мезотелиомы плевры при воздействии асбеста и т.п.
Заболевания могут быть также обусловлены нарушением баланса между внутренней и внешней средой организма, что особенно характерно для эндемических заболеваний. Этиология и патогенез некоторых эндемических заболеваний достаточно хорошо изучены. Например, установлено, что наблюдаемый во многих регионах мира флюороз обусловлен избыточным поступлением фторидов с питьевой водой; возникновение эндемического зоба связано с недостаточным содержанием йода в окружающей среде и продуктах питания и, кроме того, может быть результатом действия некоторых химических веществ, нарушающих гормональный статус.
Наиболее характерные признаки экологической, в частности химической, природы заболевания:
• внезапная вспышка нового заболевания. Нередко оно трактуется как инфекционное, и только тщательный клинический и эпидемиологический анализ позволяет выявить в качестве истинной причины воздействие химических веществ;
• патогномоничные (специфичные) симптомы. На практике этот признак встречается достаточно редко, так как специфические признаки интоксикации в основном проявляются при относительно высоких уровнях воздействия. Гораздо большее диагностическое значение имеет определенное сочетание неспецифических симптомов;
• комбинация неспецифических признаков, симптомов, данных лабораторных исследований, несвойственная известным болезням;
• отсутствие контактных путей передачи, свойственных инфекционным заболеваниям. Например, у лиц, проживающих в одной квартире с работниками асбестовых производств, очень высок риск развития опухолей легких и плевры, что обусловлено воздействием асбестовых частиц, переносимых вместе с загрязненной спецодеждой;
• общий источник воздействия у всех пострадавших; связь заболеваний с присутствием химических веществ в одном из объектов окружающей среды;
• обнаружение зависимости «доза — ответ»: увеличение вероятности развития заболевания и/или возрастание его тяжести с увеличением дозы;
• образование кластеров (сгущений) числа случаев заболеваний, обычно относительно редко встречающихся в популяции;
• характерное пространственное распределение случаев заболеваний. Географическая локализация свойственна, например, практически всем эндемическим заболеваниям;
• распределение пострадавших по возрасту, полу, социальноэкономическому статусу, профессии и другим признакам. Наиболее подверженными заболеванию часто оказываются дети, пожилые люди, больные с той или иной хронической патологией;
• обнаружение подгрупп с повышенным риском заболевания. Такие подгруппы часто могут указывать на патогенетические особенности воздействующего фактора;
• временная связь между заболеванием и воздействием факторов. Необходимо принимать во внимание возможность латентного периода, составляющего от нескольких недель (трикрезилфосфат — параличи, динитрофенол — катаракта) до нескольких десятков лет (диоксины — злокачественные новообразования);
• связь заболеваний с определенными событиями: открытием нового производства или началом выпуска (применения) новых веществ, захоронением промышленных отходов, изменением рациона питания и т.д.;
• биологическое правдоподобие: наблюдаемые изменения подтверждаются данными о патогенезе заболевания, результатами исследований на лабораторных животных;
• обнаружение в крови пострадавших исследуемого химического вещества или его метаболита;
• эффективность мер вмешательства (специфических профилактических и лечебных мероприятий).
Каждый из перечисленных выше признаков по отдельности не является определяющим, и только их совокупность позволяет заподозрить этиологическую роль факторов окружающей среды. В этом заключается чрезвычайная сложность установления экологической природы заболевания отдельного человека.
Популяционная гигиеническая диагностика используется для оценки экологической обстановки на различных территориях и выявления риска для здоровья, связанного с определенными вредными предприятиями или другими источниками загрязнения окружающей среды. Под благоприятной экологической обстановкой понимается отсутствие антропогенных источников неблагоприятных воздействий на окружающую природную среду и здоровье человека и естественных, но аномальных для данной области (региона) природноклиматических, биогеохимических и других явлений. В зависимости от интенсивности влияния факторов окружающей среды на здоровье населения выделяют зоны чрезвычайной экологической ситуации и зоны экологического бедствия.
Экологическое состояние территорий оценивается по комплексу медико-демографических показателей. В число этих показателей входят перинатальная, младенческая (в возрасте до 1 года) и детская (в возрасте 14 лет) смертность, частота врожденных пороков развития, спонтанных выкидышей, структура заболеваемости детей и взрослых и др. Наряду с показателями смертности и заболеваемости анализируют среднюю продолжительность жизни, частоту генетических нарушений в клетках человека (хромосомные аберрации, разрывы ДНК и др.), сдвиги в иммунограмме, содержание в биосубстратах (кровь, моча, волосы, зубы, слюна, плацента, женское молоко и др.) человека токсичных химических веществ.
Наряду с популяционной гигиенической диагностикой существует и индивидуальная, имеющая целью выявление причинно-следственных связей между нарушениями здоровья у конкретного человека и действующими или действовавшими в прошлом потенциально вредными факторами окружающей среды. Ее актуальность определяется не только для правильной диагностики, лечения и профилактики заболеваний, но и для установления возможной связи «среда — здоровье» с целью определения материальных компенсаций за ущерб здоровью человека в результате действия экологических или производственных факторов.
По тяжести возможные влияния на здоровье подразделяются на катастрофические (безвременная смерть, уменьшение продолжительности жизни, выраженное бессилие, инвалидизация, задержка умственного развития, врожденные уродства),тяжелые (дисфункция органов, нервной системы, дисфункция развития, поведенческие дисфункции) и неблагоприятные(похудение, гиперплазия, гипертрофия, атрофия, изменение активности ферментов, обратимая дисфункция органов и систем и др.).
Как уже было отмечено, реакции на внешнее воздействие в популяции в большинстве случаев носят вероятностный характер, что обусловлено различиями в индивидуальной чувствительности людей к действию изучаемого фактора окружающей среды. На рис. 3.9 представлен спектр биологического ответа популяции на воздействие факторов окружающей среды. Как видно из рисунка,
у наибольшей части популяции в результате экспозиции вредных факторов возникают скрытые формы заболеваний и донозологические состояния, не выявляемые по смертности, обращаемости за медицинской помощью, госпитализированной заболеваемости. Только целенаправленное и углубленное медицинское обследование способно оценить истинное состояние здоровья в экспонированной популяции. Эту задачу призвана решить гигиеническая диагностика.
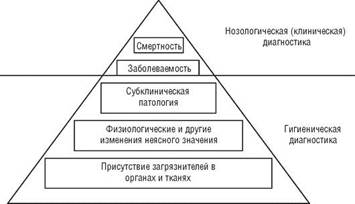
Гигиеническая диагностика делает акцент на выявлении предболезненных (преморбидных) состояний. Предмет исследования гигиенической диагностики — это здоровье, его величина. Она проводится врачом с целью оценки состояния адаптационных систем, раннего выявления напряжения или нарушения адаптационных механизмов, которые в дальнейшем могут привести к болезни. Врач не может и не должен успокаиваться даже в том случае, когда пациент пришел с определенными жалобами, но объективных признаков заболевания обнаружить у него не удалось. Следует таких людей (если только это не явные симулянты) относить в группу риска (наблюдения) и изучать состояние их здоровья в динамике.
Классификация канцерогенов (МАИР)
1 — известные канцерогены для человека; 2А — вероятные канцерогены для человека; 2Б — возможные канцерогены;
3 — агенты, не классифицируемые по канцерогенной способности;
4 — агенты, вероятно, не канцерогенные для человека.
Для многих видов злокачественных новообразований профилактические мероприятия оказываются чрезвычайно эффективными. По данным ВОЗ, профилактическими мероприятиями можно снизить риск развития рака желудка в 7,6 раза, толстой кишки — в 6,2 раза, пищевода — в 17,2 раза, мочевого пузыря — в 9,7 раза. Около 30% всех случаев смерти от всех видов злокачественных новообразований и 85% случаев от рака легких связаны с курением.
Столь широкий спектр химических факторов и производств (далеко не полный!) требует от врача иметь представление хотя бы в рамках данного списка о возможном риске для своих пациентов и ориентироваться именно на наиболее ранние признаки возможного неблагополучия в состоянии здоровья людей.
Источник
Существует целый ряд специфических заболеваний, связанных с воздействием факторов окружающей среды. Рассмотрим некоторые из этих заболеваний.
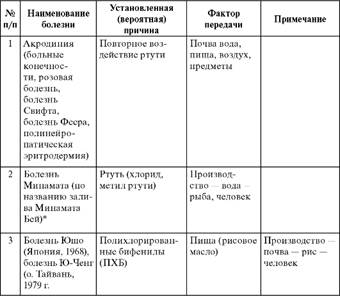
Акродиния (больные конечности, розовая болезнь, болезнь Свифта, болезнь Феера) – заболевание, обусловленное повторными воздействиями ртути. Сопровождается дегенеративными изменениями центральной нервной системы, хроматолизисом клеток коры головного мозга и мозжечка. Клинические проявления включают в себя ишемию, цианоз пальцев, повышенную потливость. Возможна гангрена пальцев.
Длительное воздействие малых доз и концентраций ртути может приводить к микромеркуриализму. Это неврастенический синдром с признаками вегетативной дисфункции, нарушения нервно-психической сферы, мелкий и частый тремор пальцев, кровоточивость десен. Первыми признаками микромеркуриализма являются повышенная утомляемость, слабость, сонливость, апатия, эмоциональная неустойчивость, головные боли, головокружения, повышенная психическая возбудимость, нарушения сердечно-сосудистой системы.
Болезнь Минимата – заболевание, наблюдавшееся с 1953 по 1966 гг. у населения, проживающего на побережье залива Минимата Бей. Связано с поступлением в залив сточных вод производства ацетальдегида и винилхлорида, содержащих ртуть.
Болезнь Минимата впервые была официально зарегистрирована в 1956 году у людей, проживающих около залива Минимата в юго-западной части Японии. В 1959 году была доказана связь заболевания с употреблением рыбы, загрязненной ртутью. Ртуть поступала в морской залив со сточными водами завода по производству ацетальдегида и поливинилхлорида. В морской воде и в водных организмах неорганическая ртуть в результате метилирования переходила в метилртуть.
В результате употребления морских продуктов в общей сложности пострадало 17 тыс. человек, у 121 пострадавшего наблюдалось острое тяжелое отравление, 46 человек умерли. Всего с 1956 года от отравления умерли 1022 человека, а 752 до сих пор страдают от его последствий. У собак, кошек, свиней, крыс и птиц, обитающих вблизи залива, развились классические клинические симптомы отравления и многие животные погибли.
Заболевание начиналось с появления чувства онемения в конечностях и в области рта, развития сенсорных расстройств, затруднения движения рук. Кроме того, у пострадавших отмечались нарушения координации движений, слабость, тремор, замедление и неясность речи, ухудшение зрения и слуха. К этим симптомам в дальнейшем присоединялись общий паралич, затруднение глотания, конвульсии. При тяжелом отравлении наступала смерть. Врожденная болезнь Минимата сходна по клинической картине с ДЦП.
Только через 40 лет после появления первых признаков экологического бедствия рыба и моллюски в заливе Минимата были признаны безопасными для здоровья.
С воздействием полихлорированных бифенилов связано развитие болезни Юшо (Япония, 1968) или болезни Ю-Ченг (Ю-Ченг, болезнь рисового масла, о. Тайвань, 1979). В японии воздействию полихлорированных бифенилов (ПХБ) подверглось 1800 человек, употреблявших в пищу рис, загрязненный трансформаторным маслом. У пострадавших только развились хлоракне. Воздействию ПХБ на острове Тайвань всего подверглось около 2000 человек. Поражение было вызвано употреблением в пищу рисового масла, загрязненного канехлором-400. ПХБ, использовавшиеся в качестве теплопроводного материала, попали в продукт в процессе производства через мельчайшие эрозированные отверстия в трубах. Ранними признаками заболевания были набухание век, пигментация ногтей и слизистых оболочек, слабость, тошнота, рвота. За этими симптомами следовали гиперкератоз, потемнение кожи с появлением хлоракне (угреподобной сыпи), часто осложнявшихся вторичной стафилококковой инфекцией. Дети, родившиеся у матерей с болезнью Юшо имели пониженную массу и длину тела. Воздействие ПХБ на плод проявилось в снижении интеллекта, гиперактивности, нарушении поведения. Изменения постепенно прогрессировали. Спустя 1-3 года в печени и крови пострадавших были обнаружены высокие концентрации ПХБ.
Период выведения ПХБ из организма составляет 58 лет. В США с 1942 года по 1982 год производственному воздействию ПХБ подверглись 6583 рабочих.
ПХБ, а также полибромированные бифенилы оказывают канцерогенное действие и влияют на репродуктивную функцию.
Одним из сильнейших канцерогенов и наиболее токсичным веществом из известных химических соединений с 1970 года признан 2,3,7,8-Тетрахлордибензо-п-диоксин (2,3,7,8-ТХДД).
Массивное воздействие диоксинов произошло 10 июля 1976 года в Севезо (Италия). В результате аварии на производстве в окружающую среду поступило, по различным оценкам, от 300 до 130 кг 2,3,7,8-ТХДД. Воздействию подверглись около 20 000 человек, у 700 из них воздействие было наиболее интенсивным. У 200 пострадавших, в том числе у 40 детей, через 2 недели после аварии появились специфические высыпания на коже – хлоракне. В ближайшее время после воздействия никаких пороков развития у новорожденных не было обнаружено. Вместе с тем, выраженные признаки отравления были обнаружены у 60 лошадей, у новорожденных жеребят наблюдались врожденные пороки развития. Позже последствия этой аварии проявились в значительных изменениях репродуктивной функции, в том числе в увеличении числа множественных пороков развития. Среди новорожденных уменьшилась доля мальчиков.
Массивное воздействие диоксинов на население Вьетнама и американских военнослужащих происходило с 1962 по 1971 год. В период военных действий над территорий Вьетнама было распылено около 86 млн. л гербицидов-дефолиантов, в том числе около 50 млн. л «оранжевого агента» (соединения 2,4-дихлорфеноксиуксусной и 2,4,5-трихлоруксусной кислот). В 1969 году появились данные, свидетельствующие о тератогенном действии 2,4,5-Т и с 1970 года производство и применение этого соединения в США было запрещено. Последующие исследования показали, что в состав оранжевого агента в виде технологической примеси входят диоксины, спонтанно образующиеся в процессе синтеза препарата. Концентрация диоксинов в гербициде составляет от 0,05 до 50 частей на миллион. Общее количество диоксинов, распыленных по Вьетнаму, оценивается 167 килограммами. Выявлена связь между воздействием оранжевого агента и риском развития саркомы мягких тканей, лимфы, появлением хлоракне.
Ежегодно только в США в окружающую среду из известных источников поступает около 14 кг диоксинов. Из 419 известных диоксинов, фуранов и бифенилов диоксиноподобная токсичность выявлена только у 30 соединений.
Отравления диоксинами проявляются хлоракне, раздражением кожи, глаз и дыхательных путей, головной болью, головокружениями, тошнотой, потерей аппетита, похуданием, повышенной утомляемостью, болями в животе и нижних конечностях, нарушениями памяти. Возможны нарушения репродуктивной функции, эмбриотропное действие, тератогенное действие. Злокачественные новообразования при действии диоксинов имеют множественную локализацию.
Болезнь Итай-Итай (кадмиевая остеомаляция) впервые описана в 1946 году в Японии у населения, употреблявшего в пищу рис, выращенный на почве, загрязненной кадмием. Этиология заболевания окончательно установлена в 1955 году. Болезнь проявляется болями в суставах, множественными переломами конечностей, повышением артериального давления, развитием нефротического синдрома. С 1955 по 1968 гг. заболело несколько сотен человек и около 100 человек умерли.
Высокие уровни загрязнения объектов окружающей среды кадмием отмечены во многих странах мира. В г. Льеже (Бельгия) высокая смертность от нефрита связана с загрязнением почвы кадмием.
Кадмий обладает также канцерогенными свойствами и увеличивает риск развития атеросклероза и гипертензии.
Среди факторов, воздействующих на здоровье населения, одно из ведущих мест занимает свинец – протоплазматический яд широкого спектра действия. Этот элемент является поведенческим тератогеном. При воздействии свинца на организм матери у родившихся детей снижен интеллект, снижена способность к обучению и отмечены нарушения поведения. Вклад свинца в развитие гипертонической болезни составляет 1-2%.
Длительное воздействие относительно высоких доз и концентраций свинца обусловливают так называемую свинцовую триаду: свинцовую кайму (темно-серая полоска по краю десны), свинцовый колорит (землисто-серый цвет лица с легкой желтушностью), свинцовую колику. Одновременно у пострадавших наблюдается изменение системы кроветворения.
Во многих странах источником свинца являются краски, в том числе используемые в жилище. В США 40 млн. домов, построенных до 1950 года и 25%, возведенных до 1975 года, стали источником воздействия свинца. По данным ВОЗ, от 15 до 20% первоклассников в США имеют признаки свинцовой интоксикации и около 200 детей ежегодно умирают вследствие свинцовых отравлений, связанных главным образом со свинец-содержащими красками.
Болезнь Кашина-Бека (уровская болезнь, эндемическая деформация) встречается в Китае, на Дальнем Востоке, в Приамурье, Читинской области. Заболевание чаще всего встречается у детей в возрасте 5-13 лет и проявляется множественными дегенерациями и некрозом суставного хряща, мышечной дистрофией, задержкой роста, деформацией скелета.
В настоящее время существует несколько гипотез развития данной болезни: действие афлатоксинов, стронция, повышенное содержание в колодезной воде гуминовых кислот, дисбаланс ряда микро- и макроэлементов.
Болезнь Кешана (крайняя форма селенодефицита) проявляется острой хронической кардиомиопатией, нарушением ритма сердца, аритмией, мышечной слабостью. Заболевание распространено в сельских районах с низким содержанием селена в окружающей среде. В 95% случаев страдают дети. При высоких уровнях селена возможен селеноз с поражением зубов, дерматитом, желудочно-кишечными нарушениями, поражением центральной нервной системы, снижением содержания гемоглобина. Возможно увеличение риска онкологических заболеваний.
Источник
