Морфологические изменения характерные для гипертонической болезни
Гипертоническая болезнь (синонимы: первичная, или эссенциальная, идиопатическая гипертензия) – хроническое заболевание, основным клиническим признаком которого является длительное и стойкое повышение артериального давления (гипертензия).
Патогенез.Ключевой признак устойчивой первичной гипертензии – это повышение периферической сосудистой резистентности. Существует множество механизмов, ведущих к развитию первичной гипертонии.
(a) натриевый гомеостаз;
(b) симпатическую нервную систему;
(c) ренин-ангиотензин-альдостероновую систему.
Натриевый гомеостаз. Отмечено, что первыми обнаруживаемыми изменениями является замедленная почечная экскреция натрия. Натриевая задержка сопровождается увеличением объема и скорости кровотока, обусловленные увеличением сердечного выброса. Периферическая ауторегуляция повышает сосудистую резистентность и в итоге обуславливает гипертонию. Известно, что повышенный переход Nа+ в эндотелиальные клетки артериальной стенки может также повышать и внутриклеточное содержание Са2+. Это способствует повышению сосудистого тонуса и отсюда, следовательно, периферического сосудистого сопротивления.
Симпатическая нервная система.Артериальное давление – это производная общего периферического сосудистого сопротивления и сердечного выброса. Оба эти показателя находятся под контролем симпатической нервной системы.
Ренин-ангиотензин-альдостероновая система.Ренин образуется в юкстагломерулярном аппарате почек, диффундирует в кровь через “выносящие артериолы”. Ренин активирует плазматический глобулин (называемый “рениновый субстрат” или ангиотензин) для высвобождения ангиотензина I. Ангиотензин I превращается в ангиотензин II под воздействием ангиотензин-трансферазы. Ангиотензин II является мощным вазоконстриктором и поэтому его повышенная концентрация сопровождается выраженной гипертензией.
Недавно выявлены ассоциации между мутациями генов, кодирующих выработку ангиотензина I, ангиотензин-трансферазы и некоторых рецепторов для ангиотензина II и развитием первичной гипертонии. Также есть связь между полиморфизмом гена, кодирующего выработку ангиотензин-трансферазы и “идиопатической” сердечной гипертрофии у больных с нормальным артериальным давлением.
Патологическая анатомия. Морфологические проявления гипертонической болезни зависят от характера и длительности ее течения. По характеру течения болезнь может протекать злокачественно (злокачественная гипертензия) и доброкачественно (доброкачественная гипертензия).
При злокачественной гипертензии доминируют проявления гипертонического криза, т.е. резкого повышения артериального давления в связи со спазмом артериол.
Морфологические проявления гипертонического криза:
1. гофрированность и деструкция базальной мембраны, расположение эндотелия в виде частокола в результате спазма артериолы;
2. плазматическое пропитывание или фибриноидный некроз ее стенки артериол;
3. тромбоз, сладж-феномен.
При этой форме часто развиваются инфаркты, кровоизлияния в различные органы.
Злокачественная артериальная гипертензия:
- Фибриноидный некроз сосудов с присоединяющимися тромбозом и связанные с ним органные изменения: инфаркты, кровоизлияния, быстро развивающаяся почечная недостаточность.
- Двусторонний отёк диска зрительного нерва, сопровождающийся белковым выпотом и кровоизлияниями в сетчатку.
- В почках развивается злокачественный артериолонекроз Фара.
Злокачественный артериолосклероз Фара (фаровская почка).
Макроскопически: поверхность почки может быть гладкой или мелкобугристой (в зависимости от длительности предсуществующей доброкачественной фазы артериальной гипертензии), характерны мелкоточечные кровоизлияния, которые придают почке пёстрый вид.
Микроскопически: фибриноидный некроз артериол и капиллярных петель клубочков, отёк интерстиция и диапедезные кровоизлияния.
При доброкачественной форме гипертонической болезни различают три стадии, имеющие определенные морфологические различия:
1) доклиническую;
2) выраженных распространенных морфологических изменений артериол и артерий;
3) вторичных изменений внутренних органов, обусловленных изменениями сосудов и нарушением внутриорганного кровообращения.
Вместе с тем, в любой стадии доброкачественной гипертензии может возникнуть гипертонический криз с характерными для него морфологическими проявлениями.
Доклиническая стадия гипертонической болезни характеризуется периодическим, временным повышением артериального давления. При микроскопическом исследовании выявляют умеренную гипертрофию мышечного слоя и эластических структур артериол и мелких артерий, спазм артериол. Клинически и морфологически обнаруживают умеренную гипертрофию левого желудочка сердца.
Стадия выраженных распространенных морфологических изменений артериол и артерий является результатом длительного повышения артериального давления. В этой стадии возникают морфологические изменения в артериолах, артериях эластического, мышечно-эластического и мышечного типов, а также в сердце.
Наиболее характерным признаком гипертонической болезни является изменения артериол. В артериолах выявляется плазматическое пропитывание, которое завершается артериолосклерозом и гиалинозом.
Плазматическое пропитывание артериол и мелких артерий развивается в связи с гипоксией, обусловленной спазмом сосудов, что влечет за собой повреждение эндотелиоцитов, базальной мембраны, мышечных клеток и волокнистых структур стенки. В дальнейшем, белки плазмы уплотняются и превращаются в гиалин. Развивается гиалиноз артериол или артериолосклероз. Наиболее часто плазматическому пропитыванию и гиалинозу подвергаются артериолы и мелкие артерии почек, головного мозга, поджелудочной железы, кишечника, сетчатки глаза, капсулы надпочечников.
В артериях эластического, мышечно-эластического и мышечного типов выявляется эластоз и эластофиброз. Эластоз и эластофиброз – это последовательные стадии процесса и представляют собой гиперплазию и расщепление внутренней эластической мембраны, которая развивается компенсаторно в ответ на стойкое повышение артериального давления. В дальнейшем происходит гибель эластических волокон и замещение их коллагеновыми волокнами, т.е. склероз. Стенка сосудов утолщается, просвет сужен, что ведет к развитию хронической ишемии в органах. В этой стадии масса сердца достигает 900–1000 г, а толщина стенки левого желудочка составляет 2–3 см. В связи с нарушением трофики миокарда (в условиях кислородного голодания) развивается диффузный мелкоочаговый кардиосклероз.
Последняя стадия гипертонической болезни или стадия вторичных изменений внутренних органов обусловлена изменениями сосудов и нарушением внутриорганного кровообращения.
Эти вторичные изменения могут проявляться либо очень быстро в результате спазма, тромбоза, фибриноидного некроза стенки сосуда и завершаются кровоизлияниями или инфарктами, либо могут развиваться медленно в результате гиалиноза и артериолосклероза и вести к атрофии паренхимы и склерозу органов.
На основании преобладания сосудистых, геморрагических, некротических и склеротических изменений в сердце, мозге, почках при гипертонической болезни выделяют сердечную, мозговую и почечную клинико-морфологические ее формы.
· Сердечная форма гипертонической болезни вместе с сердечной формой атеросклероза составляют сущность ишемической болезни сердца.
· Мозговая форма гипертонической болезни рассматривается в разделе цереброваскулярные заболевания.
· Почечная форма гипертонической болезни характеризуется как острыми, так и хроническими изменениями.
К острым изменениям относятся инфаркты почек и артериолонекроз почек, которые связаны с тромбоэмболией или тромбозом артерий. В ответ на некроз в артериолах, клубочках и строме развиваются клеточная реакция и склероз. Почки выглядят несколько уменьшенными в размерах, пестрыми, поверхность их мелкогранулярная. Наиболее характерные изменения выявляются в почках при доброкачественном течении гипертонической болезни. Эти изменения обусловлены недостаточным питанием, т.е. хронической ишемией. В результате недостаточного кровоснабжения и гипоксии канальцевая часть большинства нефронов атрофируется и замещается соединительной тканью, которая разрастается также вокруг погибших клубочков. На поверхности почек появляются мелкие множественные очаги западения. Нефроны, соответствующие относительно сохранным клубочкам, гипертрофируются и выступают над почечной поверхностью. Почки резко уменьшаются в размере (практически вдвое), плотные, поверхность их мелкозернистая, паренхима равномерно истончена, особенно корковое вещество. Масса почек может достигать 50-60 грамм. Такие почки называют первично-сморщенными. Первично – потому, что уменьшение почек происходит от нормальных размеров, в то время как во всех остальных случаях (при воспалении, дистрофических процессах) почки вначале увеличиваются в объеме, а затем вторично происходит их уменьшение. Еще одно название почек “артериоло-склеротический нефросклероз” показывает, что в основе болезни первоначально лежит поражение артериол.
· Изменения глаз при гипертонической болезни вторичные и связаны с типичными изменениями сосудов. Эти изменения проявляются в виде отека соска зрительного нерва, кровоизлияний, отслойки сетчатки, в тяжелых случаях ее некрозом и тяжелыми дистрофическими изменениями нервных клеток ганглиозного слоя.
Причины смерти. Наиболее частыми причинами смерти являются сердечная недостаточность в результате диффузного кардиосклероза (в острых случаях – инфаркт миокарда), хроническая почечная недостаточность (азотемическая уремия), кровоизлияние в мозг.
Источник
Для изучения скоропостижной смерти мы сопоставляли случаи скоропостижной и нескоропостижной смерти при одном и том же заболевании. Целью работы было изучение патологической анатомии гипертонической болезни, закончившейся острой сердечно-сосудистой недостаточностью. Всего исследовали 40 случаев. Причиной смерти в 31 наблюдении была острая сердечно-сосудистая недостаточность, в 9— инфаркт миокарда, из них 2 с разрывом и тампонадой сердца. Возраст умерших был от 31 года до 64 лет, в большинстве наблюдений — от 45 до 59 лет. Клинические данные изучали по амбулаторным картам. Давность заболевания от 3 до 8 лет. По клиническому течению это были преимущественно цереброкардиальные формы гипертонической болезни; в 14 наблюдениях гипертоническая болезнь при жизни не была диагностирована.
В ряде наблюдений накануне или в день смерти отмечено ухудшение общего состояния. Агональный период продолжался от 10 мин. до 1 часа. Для сопоставления изучено 20 случаев гипертонической болезни, закончившихся нескоропостижной смертью.
Гистологически исследовали кусочки мозга (различные отделы коры, продолговатый мозг, мозжечок, область подкорковых узлов, аммонов рог), эндокринных желез и внутренних органов. Срезы окрашивали гематоксилин-эозином, пикрофуксином, Суданом III. Для исследования нервной системы применяли специальные методы (Ниссль, Ортег, Кахаль).
В половине случаев гипертонической болезни сопутствовал общий атеросклероз; у 9 больных отмечено преимущественное поражение коронарных артерий, у 6 — сочетание атеросклероза коронарных артерий и аорты, у 5 — единичные плоские желтоватые бляшки в аорте и венечных сосудах. Возраст этих умерших от 31 года до 47 лет. Вес сердца колебался от 380 до 760 г (в среднем 500—550 г). В большинстве случаев имелся мелкоочаговый или крупноочаговый кардиосклероз, в 6— с образованием хронических аневризм. Были случаи стенозирующего атеросклероза основных ветвей коронарных артерий без макроскопически видимого кардиосклероза.
В почках лишь в 1/3 наблюдений удалось отметить мелкозернистую поверхность. В мозгу постоянно обнаруживали отек. Лишь в единичных случаях обнаружены старые кисты от размягчения в подкорковых узлах.
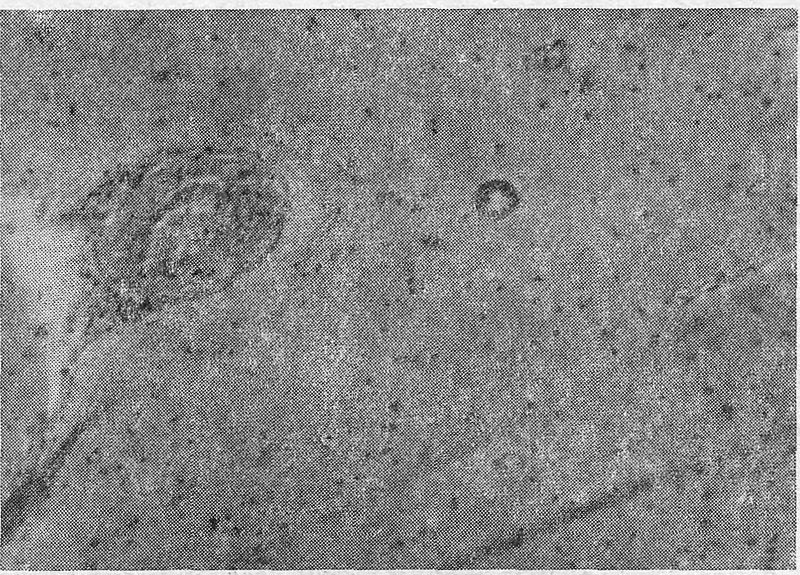
При микроскопическом исследовании первое место по частоте и распространенности изменений в сосудах занимает мозг. В нем наряду со старыми изменениями (гиалиноз сосудов оболочек и вещества мозга, отложение гемосидерина вокруг артерий и вен, очаги разрежения вещества мозга, глиозная реакция) обычно наблюдали повышение проницаемости сосудов и острые расстройства кровообращения, свойственные кризу. Из явлений нарушения проницаемости наиболее постоянны набухание стенок мелких артерий и артериол, сегментарные плазморрагии (рис. 1), иногда с образованием микроаневризм и разрывом стенок, скопления зернистых масс вокруг мелких сосудов и капилляров, распространенные периваскулярные кровоизлияния (последние часто наблюдались и вокруг вен). Наряду с этим отмечены участки неравномерного полнокровия, стазы, паретическое расширение вен, а на фоне расстройств кровообращения — морфологические изменения стромы и паренхимы мозга.

Рис. 1. Набухание и плазматическое пропитывание мелкой артерии мозга с периваскулярный отеком и «глиозной реакцией». Окраска гематоксилин-эозином. Ок. 10, об. 8.
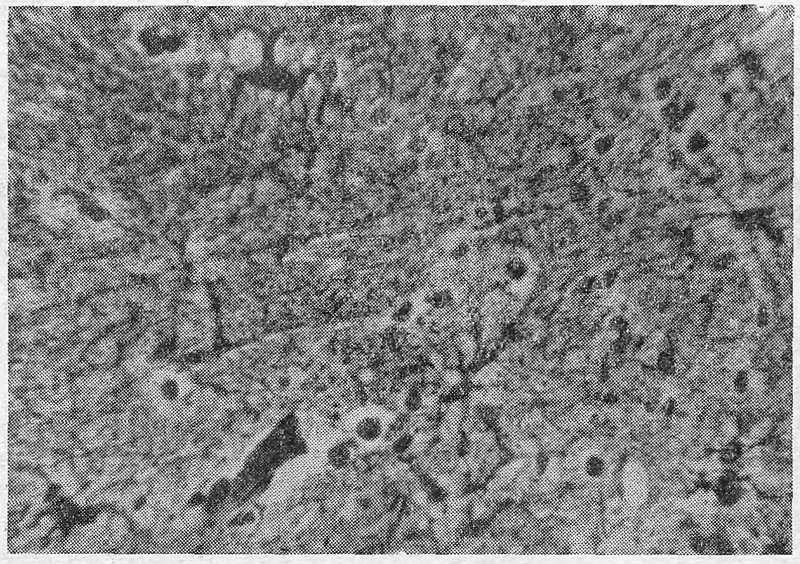
Рис. 2. Утолщение и фрагментация отростков в клетках Ортега. Импрегнация серебром по методу Ортега. Ок. 15, об. 20.
Количество гистиоцитов (клетки Ортега) в большинстве случаев было уменьшено и они подвергались деструктивным и дистрофическим изменениям — набухание перинуклеарной протоплазмы, понижение импрегнационных свойств, вакуолизация первичных и вторичных разветвлений и т.д. (рис. 2).
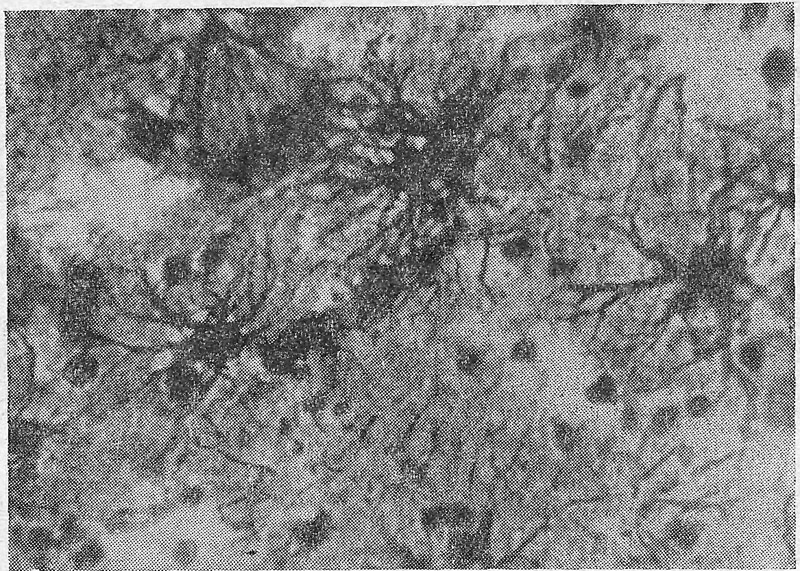
Рис. 3. Резкая гипертрофия астроцитов с огрубением отростков. Импрегнация золотом по методу Кахаля. Ок. 10, об. 40.
В олигодендроглии отмечали набухание, гипертрофию, пролиферацию. Гипертрофированные формы встречались как в белом, так и в сером веществе. В протоплазме клеток и внеклеточно находилось много аргирофильных зерен. В астроцитах имелись деструктивные и пролиферативные изменения: очаговые скопления, мелкие глиозные рубчики неодинаковой давности в различных слоях коры, крупные аргирофильные зерна в протоплазме (рис. 3). В нервных клетках обнаруживали острые и хронические изменения (растворение нисслевской субстанции, набухание, перицеллюлярный отек, сморщивание клеток и ядер, накопление липофусцина и т. д.).
В сердце преобладали изменения, имеющие давность (склероз сосудов, кардиосклероз, гипертрофия, дистрофические изменения). Морфологические признаки острой коронарной недостаточности (плазматическое пропитывание интимы крупных артерий, сегментарное плазматическое пропитывание интимы мелких артерий с образованием сосочкообразных выбуханий, отек стромы, дистрофические изменения мышечных волокон и др. ) выявлены в 23 случаях (рис. 4).
Обращая специальное внимание на сосочкообразные выбухания интимы, мы убедились, что они далеко не всегда являются следствием белкового пропитывания. На сериальных срезах было видно, что в ряде случаев они образуются в результате набухания замыкающих приспособлений артерий замыкающего типа (в них видна структура перерезанных мышечных волокон и ядер). Помимо этого, иногда сосочкообразные выбухания образуются за счет сегментарного утолщения и расщепления внутренней эластической мембраны 1. Из острых изменений чаще встречалось набухание стенок мелких артерий с частоколообразным расположением ядер эндотелия, разрыхление и отек стромы, фрагментация мышечных волокон.
В отличие от случаев, закончившихся нескоропостижной смертью, артериолосклеротические изменения в почках были выражены слабо. Гиалиноз отмечен лишь в единичных артериолах (даже в случаях гипертонической болезни у лиц старше 60 лет). Значительно чаще встречался эластофиброз средних артерий. Нефросклероз также был слабо выражен, отмечены лишь мелкие очаги его с запустеванием небольших групп клубочков под капсулой. Плазморрагии обнаружены лишь в единичных сосудах и притом не во всех наблюдениях. Из явлений повышения проницаемости значительно чаще наблюдалось скопление мелкозернистых белковых масс в капсулах клубочков. Из расстройств кровообращения можно было отметить неравномерное полнокровие коркового и мозгового слоев, резкое (часто паретическое) расширение сосудов на границе слоев и в мозговом веществе, в некоторых случаях кровоизлияния.
Наиболее часто гиалиноз и особенно плазматическое пропитывание встречались в сосудах селезенки. К гиалинозу сосудов селезенки обычно относятся скептически, считая его обычным возрастным изменением. Однако опыт изучения сосудов селезенки при травме у лиц молодого возраста показал, что ее сосуды очень быстро реагируют на травму в виде спазма и плазматического пропитывания. По-видимому, надо пересмотреть общепринятые представления о гиалинозе сосудов селезенки. Постоянно встречаясь на секционном материале, он, возможно, связан не столько с возрастом, сколько с большой реактивностью сосудов селезенки.
Гиалиноз мелких артерий печени отмечен в единичных и плазматическое пропитывание в 2 случаях. В паренхиме печени часто обнаруживали участки, состоящие из крупных клеток с разреженной крупнозернистой протоплазмой и четкими границами (напоминающие печень при шоке). Особенно демонстративны они были в наблюдениях, где смерти предшествовали эмоциональные аффекты.
Особый интерес представляло исследование эндокринных желез, поскольку они играют большую роль в адаптационных реакциях. Известно, что наступлению скоропостижной смерти часто предшествует действие внешних факторов (эмоциональные аффекты, физическая нагрузка, алкоголь), которые можно рассматривать как факторы, вызывающие в организме состояние «напряжения». С другой стороны, проявления стенокардии сами по себе являются «стрессором». Таким образом, морфологические изменения в эндокринной системе мы пытались оценить с точки зрения их участия в механизме смерти. Наибольший интерес в таком аспекте представляют надпочечники, поскольку большой экспериментальный материал, накопленный в последние годы, дает возможность судить о функциональном значении морфологических изменений и на секционном материале.
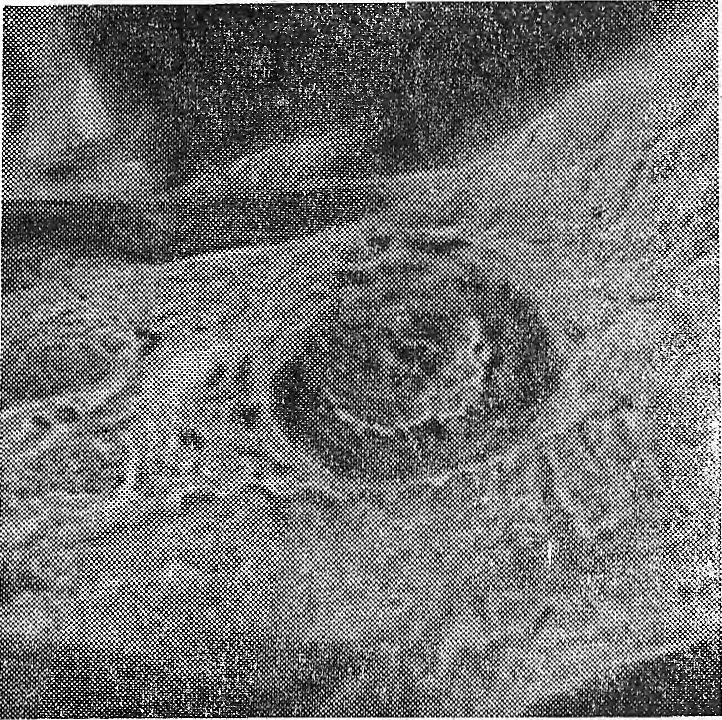
Рис. 4. Сосочкообразное выбухание интимы при инфаркте миокарда. Ок. 7, об. 40.
Надпочечники по частоте поражения сосудов занимали исключительное место наряду с мозгом. Постоянно обнаруживали гиалиноз мелких артерий, эластофиброз средних, из острых изменений — плазматическое пропитывание. Морфология коркового слоя в большей мере зависела от длительности стенокардии и продолжительности агонального периода. При быстрой смерти, когда агональный период не превышал 5—10 мин., на фоне полнокровия отмечали очаги цитолизов в пучковой зоне, кора была богата липоидами. Если смерти (за час и более) предшествовали приступы стенокардии или агональный период длился около часа, то наряду с очажками цитолизов отмечали пролиферацию зоны клубочков, утолщение пучковой зоны, небольшие фокусы делипоидизации. На подобные изменения указывает В.И. Алисиевич.
В гипофизе, особенно в случаях, где встречались изменения стенок сосудов мозга и острые расстройства кровообращения в нем, наблюдали набухание, разрыхление стенок сосудов, повышение проницаемости, кровоизлияния в ножке и на границе долей, дегрануляцию базофилов передней доли; в щитовидной железе — венозное и капиллярное полнокровие, разрыхление стенок сосудов, отек стромы, набухание замыкающих приспособлений в сосудах («сосудистые почки»), в паренхиме преобладали явления застоя. В половых железах наряду с постоянно встречающимся разрыхлением стенок мелких артерий отмечался гиалиноз и плазматическое пропитывание; в паренхиме яичек — утолщение стенок канальцев, однако явления атрофии с гиалинозом и запустеванием канальцев встречались редко. Расстройства кровообращения и различные степени аутолиза в поджелудочной железе затрудняли ее исследование.
На основании проведенного исследования видно, что патологическая анатомия гипертонической болезни, закончившейся скоропостижно острой сердечно-сосудистой недостаточностью, имеет свои особенности.
Изменения, типичные для гипертонической болезни, были менее выражены, чем в случаях нескоропостижной смерти. Реже встречались пораженные мелкие сосуды, плазматическое пропитывание с деструкцией стенок; значительно меньше были выражены склеротические процессы в строме и атрофические в паренхиме. При скоропостижной смерти на первый план выступают острые расстройства кровообращения: резкая гиперемия, стазы, кровоизлияния и др.
При анализе материала обращало на себя внимание, что острые изменения, характерные для гипертонического криза, в ряде случаев при острой сердечно-сосудистой недостаточности были более выражены в мозгу и сопровождались расстройствами кровообращения, некробиотическими изменениями макро- и микроглии и дистрофическими изменениями нервных клеток.
В сердце наблюдали морфологические признаки острой сердечно-сосудистой недостаточности, выражавшиеся сосочкообразными выбуханиями интимы мелких артерий, резким отеком стромы и т. д.
На возникновение таких выбуханий необходимо обратить особое внимание. Как уже было указано выше, они могут иметь различное происхождение, и вопрос о сущности их требует пересмотра и более детального гистологического исследования. Развивая положение о различном происхождении сосочкообразных выбуханий, мы пришли к заключению, что их возникновение может быть связано не только с коронарной недостаточностью, но и с развитием гипертонического криза в мозгу с последующим нарушением кровообращения в нем. Это положение подтверждается анализом материала, показавшим, что морфологические изменения в мозгу при острой сердечно-сосудистой недостаточности всегда имели место и иногда даже выступали на первый план, и согласуется с результатами клинико-анатомического изучения этих наблюдений, в которых неврологическая симптоматика превалировала в течении гипертонической болезни.
О том, что проявления острой сердечно-сосудистой недостаточности могут быть связаны с патологией головного мозга, убедительно говорят исследования Е.А. Савиной и В.Г. Науменко черепно-мозговой травмы.
Интересно отметить, что в 6 наблюдениях, в которых в сердце не удалось отметить признаков острой коронарной недостаточности, в мозгу отмечены нарушения проницаемости и расстройства кровообращения, характерные для гипертонического криза. Анализ этих наблюдений показал, что диагноз острой сердечно-сосудистой недостаточности как причины смерти иногда ставят без достаточных оснований, под ней может «маскироваться» гипертоническая болезнь, закончившаяся острым нарушением мозгового кровообращения без макроскопических изменений. И.В. Давыдовский также указывает, что мозговая недостаточность не всегда характеризуется кровоизлиянием в мозг или размягчением. Большее значение при сосудистых кризах имеют отек и набухание мозга в результате нарушения проницаемости сосудистых стенок. Криз может захватить большие территории мозга и выражаться отеком.
Изучение желез внутренней секреции при скоропостижной смерти показало, что они находятся в состоянии большей функциональной активности (дегрануляция базофилов передней доли гипофиза, содержание липоидов и очаги цитолизов в надпочечниках и т. д.), чем при нескоропостижной.
Подобные изменения являются отражением адаптационного синдрома и указывают на то, что железы внутренней секреции активно участвуют в приспособительных и защитных реакциях. Селье, придавая большое значение биохимическим сдвигам в миокарде, считает возможным возникновение изменений в нем (фуксинофильная дегенерация, некрозы) связать с избыточной секрецией кортикоидов во время стресса.
Таким образом, морфологические изменения в нервной и эндокринной системе играют большую роль в танатогенезе острой сердечно-сосудистой недостаточности, так как наступление внезапной смерти не всегда можно объяснить только морфологическими изменениями в сердце.
Выводы
- Морфологические изменения при скоропостижной смерти от гипертонической болезни имеют свои особенности.
- Изменения мелких артерий и артериол, свойственные гипертонической болезни, встречались в меньшем числе сосудов, реже наблюдалось плазматическое пропитывание с деструкцией сосудистых стенок, значительно слабее были выражены склеротические процессы в строме и атрофические в паренхиме по сравнению с нескоропостижной смертью.
- Первое место по степени и распространенности изменений сосудов как свежих (характерных для криза), так и имеющих давность занимает головной мозг.
- Расстройства кровообращения в мозгу, постоянно встречающиеся при острой сердечно-сосудистой недостаточности, являются одним из компонентов гипертонического криза, поскольку они сопровождаются нарушением проницаемости сосудистых стенок и реакцией глии.
- Морфологические признаки острой коронарной недостаточности могут быть связаны не только с явлениями острой сердечно-сосудистой недостаточности, но и возникать вторично в связи с изменениями в нервной системе.
- Диагноз острой сердечно-сосудистой недостаточности иногда ставят без достаточных оснований, под ним могут проходить случаи, где причиной смерти является острое нарушение мозгового кровообращения без макроскопических изменений в мозгу.
1 К.Г. Волкова подобные картины в артериолах миокарда при гипертонической болезни и выбухающие в просвет «подушечки» трактует как эластофиброз.
Источник
