Жировая болезнь печени и кардиоваскулярный риск
В статье проводится анализ патогенетических механизмов формирования сердечно-
сосудистых заболеваний у пациентов с неалкогольной жировой болезнью печени. Рассмотрена роль генетических факторов формирования атеросклероза. Показано, что наличие генотипа PNPLA3 GG связано с выраженностью атеросклеротических изменений в сонных артериях у молодых пациентов с неалкогольной жировой болезнью печени.
Неалкогольная жировая болезнь печени (НАЖБП) в настоящее время стала одной из важнейших проблем здравоохранения во всех странах мира вследствие высокой распространенности данного заболевания [1]. Распространенность НАЖБП у жителей западных стран составляет от 20 до 30%, а в странах Азии – от 5 до 18%, и с возрастом частота заболеваемости увеличивается [2]. В настоящее время НАЖБП считается компонентом метаболического синдрома (МС) [3], который является значимым фактором риска формирования сердечно-сосудистых заболеваний (ССЗ) [4].
В представленной обзорной статье проводится анализ путей взаимосвязи формирования сердечно-сосудистых осложнений и НАЖБП.
В недавно проведенном исследовании было показано, что наличие НАЖБП было связано с риском повышенной жесткости артерий у женщин в постменопаузальном периоде, при этом интересной особенностью оказалось, что данные изменения выявлялись независимо от наличия признаков МС [5]. Аналогичные результаты по выявлению высокой частоты риска формирования ССЗ у пациентов с НАЖБП без избыточной массы тела были получены и в недавно проведенном когортном исследовании [6]. По результатам данного исследования было показано, что риск возникновения ССЗ у лиц с умеренно повышенной массой тела и наличием НАЖБП был выше, чем у лиц с избыточной массой тела, но без НАЖБП. Результаты данного исследования позволили предположить, что наличие у пациентов НАЖБП играет более значимую роль в формировании ССЗ, чем просто наличие избыточной массы тела. В настоящее время ведется активный поиск возможных патогенетических механизмов, лежащих в основе данного феномена. Известно, что НАЖБП сопровождается образованием эктопического жира в ткани печени [7]. Как оказалось, эпикардиальный жир, который является классическим эктопическим жиром, связан с повышенным риском формирования ССЗ [8]. Таким образом, эктопическое накопление жировой ткани может являться ключевым патогенетическим элементом формирования ССЗ, и, следовательно, пациенты с НАЖБП имеют более высокий риск их развития [4].
Кроме того, имеются результаты исследований, показавшие, что лица с НАЖБП обладают более высокой степенью инсулинорезистентности по сравнению с пациентами без НАЖБП, даже в том случае, если имеется нормальный показатель уровня глюкозы в плазме крови натощак и при нормальных значениях показателей инсулина и липидов в сыворотке крови [9].
Существуют исследования, объясняющие патогенетические механизмы формирования связи НАЖБП и ССЗ посредством накопления жировой ткани в печени с последующим развитием гипергликемии, дислипидемии и субклинического воспаления [10]. Данная гипотеза подтверждается тем, что вырабатываемые жировой тканью печени при стеатозе адипокины, такие как адипонектин, лептин, резистин, фактор некроза опухоли альфа (ФНОα) и интерлейкин-6 [11, 12], активно принимают участие в формировании ССЗ у лиц с НАЖБП [13].
Кроме того, имеется гипотеза, что способность к хранению жировой ткани отличается у различных людей, при
этом эктопический жировой слой может легко увеличиваться у тех лиц, у которых отмечается низкая способность к накоплению и хранению подкожной жировой клетчатки и висцеральной жировой ткани [14]. Таким образом, лица с наименьшим весом в сочетании с НАЖБП представляют собой представителей классического фенотипа с низкой способностью хранить подкожный и висцеральный жир. Таким образом, риск формирования ССЗ у пациентов с умеренной массой тела в сочетании с НАЖБП значительно выше, чем у представителей других фенотипов [14].
Риск развития ССЗ при НАЖБП отличался в зависимости от уровня системного воспаления, которое является известным медиатором и биомаркером неблагоприятных исходов у пациентов [15]. Лица с НАЖБП и более высокими уровнями С-реактивного белка имели самый высокий риск формирования ССЗ, что позволяет предположить, что одновременное существование НАЖБП и системного воспаления значительно увеличивает риск развития ССЗ [16]. Данные результаты требуют более пристального внимания к молодым лицам с асимптоматическим течением НАЖБП и повышенными показателями С-реактивного белка, отражающими наличие системного воспалительного процесса, в отношении комплекса мер по рациональному питанию и физической активности для предотвращения прогрессирования НАЖБП.
Недавние исследования показали, что НАЖБП ассоциируется с высоким риском ССЗ посредством эндотелиальной дисфункции [17, 18].
Было показано, что риск ССЗ у пациентов с НАЖБП связан с увеличением толщины комплекса интима – медиа сонной артерии, которая отражает проявление субклинического атеросклероза и служит важным предиктором риска развития инфаркта миокарда и появления атеросклеротических бляшек в сонных артериях [19–21]. Выявленная взаимосвязь между увеличением толщины комплекса интима – медиа сонной артерии и наличием НАЖБП была независимо подтверждена в нескольких исследованиях, свидетельствующих о том, что наличие у пациента НАЖБП ассоциируется с увеличением толщины комплекса интима – медиа, независимо от наличия традиционных кардиометаболических факторов риска [22–24]. В работе было показано, что степень гистологических изменений в печени у пациентов с НАЖБП имела сильную корреляционную связь с проявлениями атеросклеротических изменений в сонных артериях, независимо от классических факторов риска, что указывает на то, что степень изменений в ткани печени играет важную роль в прогрессировании атеросклероза [25].
В настоящее время доказано, что у пациентов со стеатогепатозом отмечается наличие стеатоза миокарда, который является предиктором дисфункции левого желудочка [26].
Немаловажное значение в повышении риска развития ССЗ принадлежит кальцификации коронарных артерий, определяемой с помощью компьютерной томографии [27], при этом наличие у пациентов НАЖБП служит независимым фактором риска кальцификации коронарных артерий [28].
Имеются сведения, что наличие у пациентов НАЖБП независимо коррелирует с нарушением диастолической функции левого желудочка, что было показано на пациентах с НАЖБП без ожирения, артериальной гипертонии, сахарного диабета 2-го типа, у которых были выявлены нарушение геометрии левого желудочка и признаки его диастолической дисфункции [29].
Определенное значение придается повышенному риску формирования у пациентов с НАЖБП застойной сердечной недостаточности. В 2 популяционных когортных исследованиях, включавших более 7000 человек, было показано, что наличие у пациентов НАЖБП с повышением уровня трансаминаз являлось независимым фактором риска формирования сердечной недостаточности [30, 31].
Имеются данные, показавшие, что эхокардиографические признаки склеротических изменений аортального клапана имели четкую связь с наличием у пациентов НАЖБП, которая являлась независимым фактором риска данных изменений клапана [32].
В последние годы было показано, что на ранних стадиях формирования НАЖБП у пациентов выявляется увеличенное содержание клеток – предшественников эндотелина, повышение количества которых напрямую определяется степенью тяжести НАЖБП [33]. Считается, что повышение количества данных клеток возникает как результат реакции организма на повреждение эндотелия для компенсации и восстановления поврежденного эндотелия, однако данный компенсаторный механизм нестойкий и быстро истощается, приводя к прогрессированию системного эндотелиального повреждения.
Имеется исследование, показавшее, что НАЖБП является серьезным стимулом для прогрессирования инсулинорезистентности и дислипидемии с повышением продукции триглицеридов и липопротеидов низкой плотности, что является значимым фактором риска формирования и прогрессирования системных атеросклеротических проявлений [34].
Снижение выработки адипонектина, обладающего антифибротическим, антиатерогенным и противовоспалительным действием, в сочетании с повышением выработки лептина, имеющего противоположные эффекты, способствует прогрессированию стеатогепатоза в стеатогепатит и повышению риска развития ССЗ у пациентов с НАЖБП [15].
Определенное значение в развитии и прогрессировании ССЗ у пациентов с НАЖБП отводится генетическим механизмам. В частности, было показано, что наличие генотипа PNPLA3 GG (пататин-подобный домен, содержащий 3 фосфолипазу) связан с выраженностью атеросклеротических изменений в сонных артериях у молодых пациентов с НАЖБП [35]. Варианты гена PNPLA3 могут быть связаны с увеличением накопления липидов в артериальной стенке, а также индуцировать высвобождение молекулы адгезии – ICAM-1, приводя к повышению риска развития инфаркта миокарда и инсульта [36].
Кратко патогенетический механизм формирования сердечно-сосудистых осложнений представлен на рисунке 1.![Рис. 1. Патогенез формирования сердечно-сосудистых осложнений при НАЖБП [37] Рис. 1. Патогенез формирования сердечно-сосудистых осложнений при НАЖБП [37]](https://www.rmj.ru/upload/medialibrary/cab/86-1.png)
Таким образом, данные современной литературы свидетельствуют о том, что НАЖБП является независимым фактором повышенного риска формирования ССЗ, при этом риск смерти от кардиальной патологии может быть выше у пациентов с неалкогольным стеатогепатитом и выраженным фиброзом по сравнению с лицами с начальной стадией заболевания – стеатозом. Принимая во внимание столь высокий риск развития ССЗ, следует проводить пациентам с НАЖБП скрининг на наличие заболевания сердечно-сосудистой системы. И наоборот, наблюдая пациента с ССЗ, нельзя забывать о возможности наличия у него НАЖБП, которая отягощает течение кардиоваскулярной патологии. Не зря подобный «перекрестный» скрининг (у пациентов с НАЖБП на МС и ССЗ, а у пациентов с МС и/или ССЗ на НАЖБП) входит в современные международные рекомендации по диагностике и лечению НАЖБП [38]. Поэтому немедикаментозная и медикаментозная терапия пациентов с НАЖБП, особенно на этапе стеатоза, является крайне значимой в плане снижения у них риска формирования и прогрессирования сердечно-сосудистой патологии.
Источник
Неалкогольная жировая болезнь печени (НАЖБП) – наиболее частая причина хронических заболеваний печени в Российской Федерации и на Западе. НАЖБП часто ассоциирована с метаболическим синдромом и может рассматриваться как один из его компонентов. Смертность больных НАЖБП обусловлена в основном не столько прогрессированием заболевания печени как такового с развитием цирроза печени, печеночной недостаточности или гепатоцеллюлярной карциномы, как смертностью от сердечно-сосудистых заболеваний (ССЗ). В настоящем обзоре приводятся данные о связи НАЖБП и ССЗ. Большинство исследований свидетельствуют о том, что НАЖБП связана с увеличением числа ССЗ. Риск развития ССЗ увеличивается по мере прогрессирования заболевания печени. НАЖБП выступает независимым фактором, вносящим свой вклад в развитие и прогрессирование ССЗ.
Неалкогольная жировая болезнь печени (НАЖБП) включает стеатоз, неалкогольный стеатогепатит (НАСГ) и цирроз печени. Диагноз НАЖБП означает накопление липидов в печени ≥5%, по данным методов визуализации, в отсутствие других установленных причин жировой дегенерации печени, таких как прием алкоголя, вирусы, лекарственные препараты и аутоиммунные заболевания. В последнее время НАЖБП занимает лидирующее положение среди заболеваний печени. Она наблюдается у трети взрослого населения как в странах Западной Европы и США, так и в Российской Федерации. У большинства больных НАЖБП ассоциирована с метаболическим синдромом (МС) и может рассматриваться как один из его компонентов. У этих пациентов также имеются факторы риска развития сердечно-сосудистых заболеваний (ССЗ) [1–3]. НАЖБП рассматривают также как полисистемное заболевание, затрагивающее различные органы, в т.ч. и сердечно-сосудистую систему [3]. В настоящее время широко обсуждается роль НАЖБП как независимого фактора риска развития ССЗ и повышения смертности от ССЗ.
НАЖБП повышает показатель общей смертности на 57%, главным образом в связи с ССЗ или патологией печени [4].
Всесторонний мета-анализ 27 перекрестных исследований позволил выявить сильную связь между НАЖБП и некоторыми маркерами субклинического течения атеросклероза, такими как увеличение толщины комплекса интима-медиа сонных артерий (16 исследований), увеличение кальцификации коронарных артерий (7 исследований), нарушение вазодилатации (7 исследований) и жесткость артерий (6 исследований). Причем эта связь не зависела от классических факторов риска ССЗ и признаков МС у пациентов [5].
Исследование, проведенное в США и охватившее более 11 тыс. взрослых, показало, что НАЖБП связана с повышенной распространенностью ССЗ независимо от многочисленных факторов риска ССЗ [6]. В то же время авторами сделан вывод, согласно которому НАЖБП не является прогностическим фактором риска общей смертности и смертности от различных заболеваний, по данным 14-летнего периода наблюдения, что могло быть связано с включением в контрольную группу лиц с незначительно выраженным стеатозом. Анализ этой базы данных, проведенный позднее, выявил, что выраженный фиброз при НАЖБП независимо связан с увеличением общей смертности на 69% в основном за счет смертности от ССЗ [7].
При сахарном диабете 2 типа (СД2) заболевания коронарных и церебральных артерий чаще встречаются при наличии НАЖБП независимо от традиционных факторов риска ССЗ и применения лекарственных препаратов. При анализе данных пациентов, направленных на проведение коронарографии, оказалось, что НАЖБП независимо связана с более тяжелым течением ишемической болезни сердца – ИБС [8].
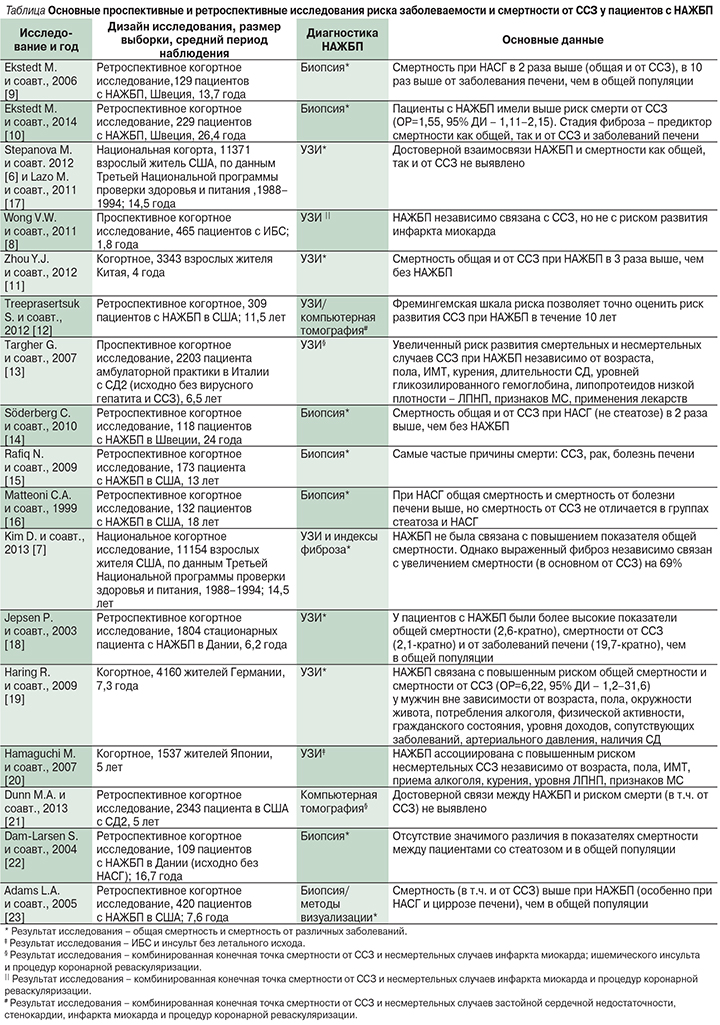
Данные ретроспективных и проспективных исследований, оценивавших связь между НАЖБП и риском развития ССЗ [6, 8–23], приведенные в таблице, в большинстве своем подтверждают, что ССЗ представляют собой серьезную угрозу для пациентов с НАЖБП.

Исследования, в которых диагноз НАЖБП ставился на основании повышения уровня печеночных проб, т.е. суррогатных маркеров заболевания, показали, что умеренное повышение уровня печеночных проб служит независимым предиктором развития ССЗ как у мужчин, так и у женщин [3, 24].
Ретроспективные исследования, в которых НАЖБП диагностировали по данным биопсии печени, свидетельствуют о том, что общая смертность, смертность от ССЗ и заболевания печени были значительно выше у пациентов с НАЖБП, чем в контрольной группе. Оказалось, что наличие и степень тяжести фиброза печени служат основным фактором, определяющим смертность этих больных. Кроме того, очень часто причиной их смерти выступали ССЗ. Именно пациенты с НАСГ, а не с простым стеатозом имеют повышенный по сравнению с референсной группой риск смерти как общей, так и от ССЗ [9, 14].
Исследования, в которых диагноз НАЖБП устанавливался на основании данных методов визуализации, показали, что НАЖБП связана с повышенным риском развития ССЗ вне зависимости от установленных факторов риска ССЗ и наличия СД2.
Мета-анализ, опубликованный в 2011 г., показал, что у пациентов с НАЖБП риск развития ССЗ в два раза выше, чем в контрольной группе (относительный риск [ОР]=2,05, 95% доверительный интервал [ДИ] – 1,81–2,31), однако смертность от ССЗ не определяется выраженностью гистологических изменений в печени [4].
Данные ряда исследований подтверждают, что НАЖБП связана с изменениями метаболизма миокарда. Так, по данным магнитно-резонансной томографии (МРТ), у молодых людей с НАЖБП без ожирения, СД, с нормальными показателями артериального давления имело место нарушение метаболизма энергии в миокарде и избыточное отложение жира в эпикарде по сравнению с контрольной группой. Что любопытно: эти изменения не сопровождались структурными аномалиями миокарда левого желудочка (ЛЖ) и изменениями систолы или диастолы [25]. Оказалось, что у пациентов с СД2 с более высоким содержанием липидов в печени, по данным магнитно-резонансной спектроскопии, инсулинорезистентность миокарда выше, а перфузия ниже по сравнению с пациентами с меньшим содержанием жира в печени [26]. Более значимое накопление липидов в миокарде (стеатоз сердца) отмечен у пациентов с более выраженным накоплением липидов в печени. Стеатоз сердца оказался предиктором диастолической дисфункции ЛЖ [26].
Масса публикаций посвящена связи НАЖБП и структурных и функциональных аномалий сердца как при наличии признаков МС, так и без таковых [24]. Описаны значительные изменения структуры сердца и признаки ранней диастолической дисфункции ЛЖ при НАЖБП по сравнению с контрольной группой в отсутствие изменений метаболизма миокарда или явного заболевания сердца [27]. У пациентов с СД2 и НАЖБП без ССЗ обнаружены ранние признаки диастолической дисфункции ЛЖ при нормальной структуре сердца и систолической функции ЛЖ [28]. Выраженность диастолической дисфункции коррелировала со степенью тяжести НАЖБП, по данным ультразвукового исследования (УЗИ), независимо от наличия артериальной гипертензии, уровня контроля гликемии и других сопутствующих факторов риска ССЗ [28]. По данным корейских авторов, НАЖБП связана с диастолической дисфункцией ЛЖ независимо от признаков МС и других установленных факторов риска ССЗ [29].
Изменения со стороны миокарда возникают задолго до развития цирроза и портальной гипертензии у больных НАЖБП, следовательно, изменения со стороны сердца могут и не быть следствием изменений внутрипеченочной гемодинамики. У пациентов с НАЖБП отмечаются ранние изменения субстратного метаболизма миокарда (нарушение метаболизма высокоэнергетических фосфатов, инсулинорезистентность), что вызывает функциональные и структурные изменения сердца (дисфункцию и гипертрофию ЛЖ), потенциально с повышенным риском застойной сердечной недостаточности у этих больных. Как было показано S.G. Wannamethee, сердечная недостаточность чаще возникает при наличии НАЖБП [30].
Фрамингемское исследование продемонстрировало, что незначительное повышение уровня печеночных трансаминаз независимо связано с повышенной частотой развития такого грозного осложнения, как фибрилляции предсердий (ФП) [31]. Аналогичная связь между повышенными уровнями ферментов в сыворотке и риском ФП была отмечена в большом проспективном исследовании, включившем более 9000 человек, которые находились под наблюдением в среднем в течение 12 лет [32]. В исследовании случай/контроль обнаружено, что НАЖБП связана с повышенной распространенностью ФП у пациентов с СД2 и эта связь не зависела от клинических факторов риска ФП [33]. В проспективном исследовании обнаружено, что у пациентов с СД2 и НАЖБП в течение 10-летнего периода наблюдения чаще развивается ФП, чем у пациентов без НАЖБП. Риск развития ФП при НАЖБП был повышен в 5 раз независимо от наличия признаков МС и других факторов риска ФП [34].
НАЖБП также независимо связана с удлинением интервала QT, значимого прогностического фактора желудочковых аритмий и внезапной сердечной смерти, что также может отчасти объяснять повышенную смертность от ССЗ при НАЖБП [35].
Последний мета-анализ G. Targher и соавт., опубликованный в 2016 г., обобщил данные 16 проспективных и ретроспективных исследований с общим числом участников более 34 тыс. человек (36,3% с НАЖБП, медиана наблюдения – 6,9 года) [36]. Авторы пришли к выводу, что НАЖБП связана с увеличением числа ССЗ как со смертельным исходом, так и без такового. Риск развития ССЗ увеличивался по мере прогрессирования заболевания печени. Наблюдательный дизайн проанализированных исследований не позволил получить доказательств того, что жировая болезнь печени служит причиной развития ССЗ.
Таким образом, приведенные в обзоре данные свидетельствуют о тесной взаимосвязи НАЖБП, ССЗ и смертности от ССЗ. НАЖБП выступает независимым фактором, вносящим свой вклад в развитие и прогрессирование ССЗ, в т.ч. и в формирование структурно-функциональных нарушений сердца (дисфункции и гипертрофии ЛЖ, ФП и пр.). Клиницистам целесообразно не только сосредоточивать усилия на заболевании печени у пациентов с НАЖБП, но и проводить раннюю оценку факторов риска ССЗ с целью их возможной модификации. Также важно и, наоборот, занимаясь пациентом с ССЗ, не забывать о возможности наличия у него НАЖБП, которая отягощает течение кардиоваскулярной патологии. Поэтому с клинической точки зрения, диагностировав НАЖБП у такого пациента, необходимо назначить соответствующую терапию и для печени. Не зря подобный «перекрестный» скрининг (у пациентов с НАЖБП на МС и ССЗ, а у пациентов с МС и/или ССЗ на НАЖБП) входит в современные международные рекомендации по диагностике и лечению НАЖБП [37]. В дальнейшем для точной оценки причинно-следственных взаимосвязей НАЖБП и ССЗ и рассмотрения механизмов развития этих связей нужны дополнительные контролируемые проспективные исследования.
1. Ивашкин В.Т., Маевская М.В., Павлов Ч.С., Тихонов И.Н., Широкова Е.Н., Буеверов А.О., Драпкина О.М., Шульпекова Ю.О., Цуканов В.В., Маммаев С.Н., Маев И.В., Пальгова Л.К. Клинические рекомендации по диагностике и лечению неалкогольной жировой болезни печени Российского общества по изучению печени и Российской гастроэнтерологической ассоциации. Рос. журн. гастроэнтерол., гепатол., колопроктол. 2016;26(2):24–42.
2. Anstee Q.M., Targher G., Day C.P. Progression of NAFLD to diabetes mellitus, cardiovascular disease or cirrhosis. Nat. Rev. Gastroenterol. Hepatol. 2013;10:330–44.
3. Targher G., Day C.P., Bonora E. Risk of cardiovascular disease in patients with nonalcoholic fatty liver disease. N. Engl. J. Med. 2010;363:1341–50.
4. Musso G., Gambino R., Cassader M., Pagano G. Meta-analysis: natural history of non-alcoholic fatty liver disease (NAFLD) and diagnostic accuracy of noninvasive tests for liver disease severity. Ann. Med. 2011;43:617–49.
5. Oni E.T., Agatston A.S., Blaha M.J., Fialkow J., Cury R., Sposito A. A systematic review: burden and severity of subclinical cardiovascular disease among those with nonalcoholic fatty liver; should we care? Atherosclerosis. 2013;230:258–67.
6. Stepanova M., Younossi Z.M. Independent association between nonalcoholic fatty liver disease and cardiovascular disease in the US population. Clin. Gastroenterol. Hepatol. 2012;10:646–50.
7. Kim D., Kim W.R., Kim H.J., Therneau T.M. Association between noninvasive fibrosis markers and mortality among adults with nonalcoholic fatty liver disease in the United States. Hepatology. 2013;57:1357–65.
8. Wong V.W., Wong G.L., Yip G.W., Lo A.O., Limquiaco J., Chu W.C. Coronary artery disease and cardiovascular outcomes in patients with non-alcoholic fatty liver disease. Gut. 2011;60:1721–27.
9. Ekstedt M., Franzen L.E., Mathiesen U.L., Thorelius L., Holmqvist M., Bodemar G. Long-term follow-up of patients with NAFLD and elevated liver enzymes. Hepatology. 2006;44:865–73.
10. Ekstedt M., Hagstrom H., Nasr P., Fredrikson M., Stal P., Kechagias S. Fibrosis stage is the strongest predictor for disease-specific mortality in NAFLD after up to 33 years of follow-up. Hepatology. 2014. https:// dx.doi.org/10.1002/hep.27368,
11. Zhou Y.J., Li Y.Y., Nie Y.Q., Huang C.M., Cao C.Y. Natural course of nonalcoholic fatty liver disease in southern China: a prospective cohort study. J. Dig. Dis. 2012;13:153–60.
12. Treeprasertsuk S., Leverage S., Adams L.A., Lindor K.D., St S.J., Angulo P. The Framingham risk score and heart disease in nonalcoholic fatty liver disease. Liver. Int. 2012;32:945–50.
13. Targher G., Bertolini L., Rodella S., Tessari R., Zenari L., Lippi G.,. Nonalcoholic fatty liver disease is independently associated with anincreased incidence of cardiovascular events in type 2 diabetic patients. Diabetes Care. 2007;30:2119–21.
14. Soderberg C., Stal P., Askling J., Glaumann H., Lindberg G., Marmur J., Decreased survival of subjects with elevated liver function tests during a 28-year follow-up. Hepatology. 2010;51:595–602.
15. Rafiq N., Bai C., Fang Y., Srishord M., McCullough A., Gramlich T. Long term follow-up of patients with nonalcoholic fatty liver. Clin. Gastroenterol. Hepatol. 2009;7:234–38.
16. Matteoni C.A., Younossi Z.M., Gramlich T., Boparai N., Liu Y.C., McCullough A.J. Nonalcoholic fatty liver disease: a spectrum of clinical and pathological severity. Gastroenterology. 1999;116:1413–19.
17. Lazo M., Hernaez R., Bonekamp S., Kamel I.R., Brancati F.L., Guallar E. Nonalcoholic fatty liver disease and mortality among US adults: prospective cohort study. BMJ. 2011;343:d6891.
18. Jepsen P., Vilstrup H., Mellemkjaer L., Thulstrup A.M., Olsen J.H., Baron J.A. Prognosis of patients with a diagnosis of fatty liver–a registry-based cohort study. Hepatogastroenterology. 2003;50:2101–104.
19. Haring R., Wallaschofski H., Nauck M., Dorr M., Baumeister S.E., Volzke H. Ultrasonographic hepatic steatosis increases prediction of mortality risk from elevated serum gamma-glutamyl transpeptidase levels. Hepatology. 2009;50:1403–11.
20. Hamaguchi M., Kojima T., Takeda N., Nagata C., Takeda J. Sarui Nonalcoholic fatty liver disease is a novel predictor of cardiovascular disease. World J. Gastroenterol. 2007;13:1579–84.
21. Dunn M.A., Behari J., Rogal S.S., O’Connell M.R., Furlan A., Aghayev A. Hepatic steatosis in diabetic patients does not predict adverse liver-related or cardiovascular outcomes. Liver Int. 2013;33:1575–82.
22. Dam-Larsen S., Franzmann M., Andersen I.B., Christoffersen P., Jensen L.B., Sorensen T.I. Long term prognosis of fatty liver: risk of chronic liver disease and death. Gut. 2004;53:750–55.
23. Adams L.A., Lymp J.F., St S.J., Sanderson S.O., Lindor K.D., Feldstein A. The natural history of nonalcoholic fatty liver disease: a population-based cohort study. Gastroenterology. 2005;129:113–21.
24. Ballestri S., Lonardo A., Bonapace S., Byrne C.D., Loria P., Targher G. Risk of cardiovascular, cardiac and arrhythmic complications in patients with nonalcoholic fatty liver disease. World J. Gastroenterol. 2014;20:1724–45.
25. Perseghin G., Lattuada G., De C.F., Esposito A., Belloni E., Ntali G. Increased mediastinal fat and impaired left ventricular energy metabolism in young men with newly found fatty liver. Hepatology. 2008;47:51–8.
26. Rijzewijk L.J., van der Meer R.W., Smit J.W., Diamant M., Bax J.J., Hammer S. Myocardial steatosis is an independent predictor of diastolic dysfunction in type 2 diabetes mellitus. J. Am. Coll. Cardiol. 2008;52:1793–99.
27. Hallsworth K., Hollingsworth K.G., Thoma C., Jakovljevic D., Macgowan G.A., Anstee Q.M. Cardiac structure and function are altered in adults with non-alcoholic fatty liver disease. J. Hepatol. 2013;58:757–62.
28. Bonapace S., Perseghin G., Molon G., Canali G., Bertolini L., Zoppini G. Nonalcoholic fatty liver disease is associated with left ventricular diastolic dysfunction in patients with type 2 diabetes. Diabetes Care. 2012;35:389–95.
29. Kim N.H., Park J., Kim S.H., Kim Y.H., Kim D.H., Cho G.Y. Non-alcoholic fatty liver disease, metabolic syndrome and subclinical cardiovascular changes in the general population. Heart. 2014;100:938–43.
30. Wannamethee S.G., Whincup P.H., Shaper A.G., Lennon L., Sattar N. Gammaglutamyltransferase, hepatic enzymes, and risk of incident heart failure in older men. Arterioscler. Thromb. Vasc. Biol. 2012;32:830–85.
31. Sinner M.F., Wang N., Fox C.S., Fontes J.D., Rienstra M., Magnani J.W. Relation of circulating liver transaminase concentrations to risk of new onset atrial fibrillation. Am. J. Cardiol. 2013;111:219–24.
32. Alonso A., Misialek J.R., Amiin M.A., Hoogeveen R.C., Chen L.Y., Agarwal S.K. Circulating levels of liver enzymes and incidence of atrial fibrillation: the Atherosclerosis Risk in Communities cohort. Heart. 2014;100:1151–56.
33. Targher G., Mantovani A., Pichiri I., Rigolon R., Dauriz M., Zoppini G. Nonalcoholic fatty liver disease is associated with an increased prevalence of atrial fibrillation in hospitalized patients with type 2 diabetes. Clin. Sci. (Lond). 2013;125:301–9.
34. Targher G., Valbusa F., Bonapace S., Bertolini L., Zenari L., Rodella S. Nonalcoholic fatty liver disease is associated with an increased incidence of atrial fibrillation in patients with type 2 diabetes. PLoS One. 2013;8:e57183.
35. Targher G., Valbusa F.., Bonapace S., Bertolini L., Zenari L., Pichiri I. Association of nonalcoholic fatty liver disease with QTc interval in patients with type 2 diabetes. Nutr. Metab. Cardiovasc. Dis. 2014;24:663–69.
36. Targher G., Byrne C., Lonardo A., Zoppini G., Barbiu C. Nonalcoholic fatty liver disease and risk of incident cardiovascular disease: a meta-analysis. J. Hepatol. 2016;65:589–600.
37. EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease. J. Hepatol. 2016;64(6):1388–402.
Е.Н. Широкова – д.м.н., проф. кафедры пропедевтики внутренних болезней лечебного факультета ФГБОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России, Москва; e-mail: elshirokova@yandex.ru
Источник
